
| 实验 序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A、C>1.0 |
| B、实验2可能使用了催化剂 |
| C、实验3比实验2先达到化学平衡状态 |
| D、前10分钟,实验4的平均化学反应速率比实验1的大 |
| 1.0mol/L-0.8mol/L |
| 10min |
| 1.0mol/L-0.4mol/L |
| 10min |


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
| A、NO2--酸性氧化物 Na2O2--碱性氧化物 Al2O3--两性氧化物 |
| B、汽油--混合物 胆矾--纯净物 H2--单质 |
| C、苏打--碱 硫化氢--酸 小苏打--酸式盐 |
| D、液氯--非电解质 硫酸钡--强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
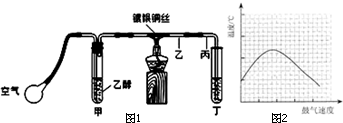 某课外活动小组利用如图1装置进行乙醇的催化氧化实验并制取乙醛(试管丁中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的镀银铜丝,约lmin后鼓入空气.请填写下列空白:
某课外活动小组利用如图1装置进行乙醇的催化氧化实验并制取乙醛(试管丁中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的镀银铜丝,约lmin后鼓入空气.请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4或NaOH |
| B、H2SO4或HCl |
| C、Na2SO4或NaCl |
| D、KOH或CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
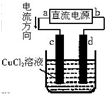 如图是电解200mL 1mol?L-1 CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
如图是电解200mL 1mol?L-1 CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )| A、a为负极,b为正极 |
| B、a为阳极,b为阴极 |
| C、电解过程中,c电极质量减少、d电极质量增加 |
| D、如果阴极上有1.6 g铜析出,则阳极上产生气体的体积(标准状况)约为0.56 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com