
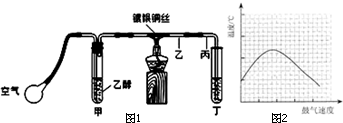
 某课外活动小组利用如图1装置进行乙醇的催化氧化实验并制取乙醛(试管丁中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的镀银铜丝,约lmin后鼓入空气.请填写下列空白:
某课外活动小组利用如图1装置进行乙醇的催化氧化实验并制取乙醛(试管丁中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的镀银铜丝,约lmin后鼓入空气.请填写下列空白:| Cu |
| △ |
| Cu |
| △ |


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
| A、过量氯气通入碘化亚铁溶液中:Cl2+Fe2++2I-=2Cl-十Fe3++I2 |
| B、向NaHCO3溶液中加入少量澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32- |
| C、H218O中投入少量Na2O2固体:2H218O+2 Na2O2=4Na++4OH-+18O2↑ |
| D、向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol/L氯化铜溶液中的Cu2+数小于NA |
| B、标准状况下,22.4 L Cl2参加任何化学反应转移的电子数都是2NA |
| C、常温常压下,16g氧气和16g臭氧(O3)所含有的氧原子数均为NA |
| D、1 mol CH5+所含电子数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| B、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C、碳酸钙溶于稀盐酸中CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、VSEPR模型就是分子的空间构型 |
| B、在共价化合物分子中一定存在σ键 |
| C、全由非金属元素组成的化合物一定是共价化合物 |
| D、共价键键长越短,键能一定越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A、C>1.0 |
| B、实验2可能使用了催化剂 |
| C、实验3比实验2先达到化学平衡状态 |
| D、前10分钟,实验4的平均化学反应速率比实验1的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
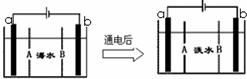 电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是
电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com