
����Ŀ����֪A�������������������Ľ�����BΪ����ɫ��ĩ���ڳ�����CΪ��ɫҺ�壬E��G��H��I��JΪ���壬����HΪ����ɫ������Ϊ��ɫ��J��ʹʪ��ĺ�ɫʯ����ֽ������ͼ�в��ֲ�������ȥ����
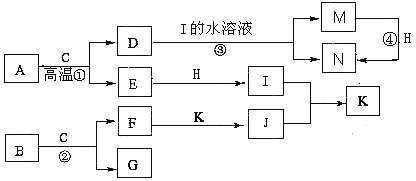
����д���пհ�
��1��д����ѧʽ��M______��K______��
��2��д�����Ļ�ѧ����ʽ_________________________________��д���������ӷ���ʽ_________________________________��
��3����Ӧ���������к��ַ�Ӧ����______������ĸ��ţ���
A�����Ϸ�Ӧ B��������ԭ��Ӧ C�����ӷ�Ӧ D���û���Ӧ
��4����Ҫȷ������Ӧ��������Һ�к���M���ʣ���ѡ�Լ�Ϊ______������ţ���
A��KSCN��Һ����ˮ B�����ۺ�KSCN C��Ũ��ˮD�����Ը��������Һ
��5�������£�H�������J��Ӧ����Ũ��İ��̣���һ�������ǿ�������Ҫ�ɷ�֮һ����д���÷�Ӧ�Ļ�ѧ����ʽ_________________________________��
���𰸡�FeCl2NH4C13Fe+4H2O![]() Fe3O4+4H2Fe3O4+8H+=Fe2++2Fe3++4H2OABCD8NH3+3Cl2= 6NH4Cl+ N2
Fe3O4+4H2Fe3O4+8H+=Fe2++2Fe3++4H2OABCD8NH3+3Cl2= 6NH4Cl+ N2
��������
��֪A�������������������Ľ�����ӦΪFe��BΪ����ɫ��ĩ��ӦΪNa2O2���ڳ�����CΪ��ɫҺ�壬ӦΪH2O����DΪFe3O4��EΪH2��GΪO2��FΪNaOH��HΪ����ɫ���壬ӦΪCl2����IΪHCl��J��ʹʪ��ĺ�ɫʯ����ֽ������ӦΪNH3����KΪNH4Cl��MΪFeCl2��NΪFeCl3��
��1�������Ϸ�����֪MΪFeCl2��KΪNH4Cl��
��2����Ӧ��������ˮ������Ӧ�����������������������仯ѧ����ʽΪ3Fe+4H2O![]() Fe3O4+4H2 ����Ӧ�������������ܽ���ϡ���������Ȼ������Ȼ��������ܽ⣬��Ӧ�����ӷ���ʽΪFe3O4+8H+=Fe2++2Fe3++4H2O��
Fe3O4+4H2 ����Ӧ�������������ܽ���ϡ���������Ȼ������Ȼ��������ܽ⣬��Ӧ�����ӷ���ʽΪFe3O4+8H+=Fe2++2Fe3++4H2O��
��3����Ӧ��Ϊ2Fe2++Cl2=2Fe3++2Cl-���÷�ӦΪ���Ϸ�Ӧ��������ԭ��Ӧ�����ӷ�Ӧ���ʴ�ΪABC��
��4������Ӧ��������Һ�к���Fe2+���������Ը��������Һ����������ԭ��Ӧ��ʹ���������Һ��ɫ������ѡ���֤���������ų������ӵĸ��ţ��ʴ�ΪD��
��5�������£�H�������J��Ӧ����Ũ��İ��̣���һ�������ǿ�������Ҫ�ɷ�֮һ���÷�Ӧ�ķ���ʽΪ8NH3+3Cl2=N2+6NH4Cl��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ƿ��������������������ȷŨ����Һ��������������������Һ���������������ȣ���ʹ��֮ǰҪ����Ƿ�©ˮ����Щ��������ȷ����( ��
A. �٢ڢۢ� B. �ڢ� C. �٢ڢ� D. �ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ҫ��������л�ѧ����ʽ�����ӷ���ʽ
��1��������������������Һ��Ӧ_______________________
��2����ҵ�ý�̿����������ƴֹ�_______________________
��3���������������������ȷ�Ӧ_______________________
��4��Na2O2��ˮ��Ӧ�����ӷ���ʽ_______________________
��5���Ȼ�������Һ��������Ӧ�����ӷ���ʽ_______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У���ȷ����
A. ͨ��ʯ�ͷ�����Ի�ô����ķ�����
B. ʯ���ѻ���Ŀ����Ϊ�˵õ���ϩ����ϩ�ͱ�
C. ú�ĸ������˻�ѧ�仯
D. ú�к��б��ͼױ�������ͨ���ȸ�������ķ����õ����ͼױ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���о���һ������Ȼ��Ϊȼ�ϵġ�ȼ��ǰ����ϵͳ�������������ͼ��ʾ����(����������δ���)��

��1����֪:CH4��CO��H2��ȼ���ȷֱ�Ϊ890.3 kJ��mol-1��283.0 kJ��mol-1��285.8 kJ��mol-1�������������е�һ����Ӧ2CH4(g)+O2(g)=2CO(g)+4H2(g) ��H�� ��
��2����ҵ�Ͽ���H2��CO2�Ʊ��״����䷴ӦΪ��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)��ij�¶��£���1 mol CO2��3 mol H2������������2 L�ܱ������У�����������Ӧ����ò�ͬʱ�̷�Ӧǰ���ѹǿ��ϵ���£�
CH3OH(g)+H2O(g)��ij�¶��£���1 mol CO2��3 mol H2������������2 L�ܱ������У�����������Ӧ����ò�ͬʱ�̷�Ӧǰ���ѹǿ��ϵ���£�

�� ��H2 ��ʾǰ2 hƽ����Ӧ����v(H2)�� ��
�� ���¶���CO2��ƽ��ת����Ϊ ��
��3����300 ����8 MPa�£���������̼�����������ʵ���֮��Ϊ1��3ͨ��һ�ܱ������з���(2)�з�Ӧ���ﵽƽ��ʱ����ö�����̼��ƽ��ת����Ϊ50%����÷�Ӧ�����µ�ƽ�ⳣ��Kp�� (��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�������)��
��4��CO2��������ɺϳɵ�̼ϩ����2CO2(g)+6H2(g)![]() CH4(g)+4H2O(g) ��H����0.1 MPaʱ����n(CO2)��n(H2)��1��3Ͷ�ϣ���ͼ��ʾΪ��ͬ�¶�(T)�£�ƽ��ʱ������̬���ʵ����ʵ���(n)��ϵ��
CH4(g)+4H2O(g) ��H����0.1 MPaʱ����n(CO2)��n(H2)��1��3Ͷ�ϣ���ͼ��ʾΪ��ͬ�¶�(T)�£�ƽ��ʱ������̬���ʵ����ʵ���(n)��ϵ��

���÷�Ӧ�Ħ�H 0(�����������������)��
������c��ʾ������Ϊ ��
��Ϊ���H2��ƽ��ת���ʣ����ı��¶��⣬���ɲ�ȡ�Ĵ�ʩ�� ����ƽ���ƶ�ԭ��˵������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.1molMg ��Al���������100mL3mol/LHCl�У��ٵμ�1mol/LNaOH ��Һ���ڵμ�NaOH��Һ�Ĺ����У�����������m��NaOH��Һ���V�仯��ͼ��ʾ��
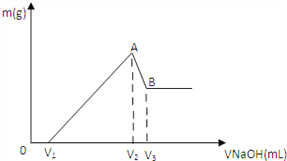
��1��д��A��B�η�Ӧ�����ӷ���ʽ_____________��
��2��A������������ʵ���n= _________________��
��3����ʹMg2+ ��Al3+�պó�����ȫ�������NaOH��Һ�����Ϊ����___________mL��(д��������̣���ͬ)
��4����V1=60mL����������Mg�����ʵ���Ϊ����___________�� V3������NaOH��Һ�����Ϊ����___________mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2�����ܱ�������,�������·�Ӧ: 2A(g)+ B(g) ![]() 2C(g)+D(g) ������������A��B����4 mol����ǰ10����A��ƽ����Ӧ�ٶ�Ϊ0.12 mol/��L������10����ʱ��������B�����ʵ����� ( )
2C(g)+D(g) ������������A��B����4 mol����ǰ10����A��ƽ����Ӧ�ٶ�Ϊ0.12 mol/��L������10����ʱ��������B�����ʵ����� ( )
A��1.6 mol B��2.8 mol C��2.4 mol D��1.2 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����a��ʾ���ȷ�Ӧ�� ��
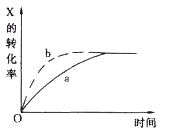
X��g��+Y��g��![]() Z��g��+M��g��+N��s�����й�����X��ת������ʱ��仯�Ĺ�ϵ����Ҫ�ı���ʼ������ʹ��Ӧ���̰�b���߽��У��ɲ�ȡ�Ĵ�ʩ���� ��
Z��g��+M��g��+N��s�����й�����X��ת������ʱ��仯�Ĺ�ϵ����Ҫ�ı���ʼ������ʹ��Ӧ���̰�b���߽��У��ɲ�ȡ�Ĵ�ʩ���� ��
A�������¶� B���Ӵ�X��Ͷ���� C���Ӵ��� D���������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com