
【题目】科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示部分(条件及物质未标出)。

(1)已知:CH4、CO、H2的燃烧热分别为890.3 kJ·mol-1、283.0 kJ·mol-1、285.8 kJ·mol-1,则上述流程中第一步反应2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH= 。
(2)工业上可用H2和CO2制备甲醇,其反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:

① 用H2 表示前2 h平均反应速率v(H2)= 。
② 该温度下CO2的平衡转化率为 。
(3)在300 ℃、8 MPa下,将二氧化碳和氢气按物质的量之比为1∶3通入一密闭容器中发生(2)中反应,达到平衡时,测得二氧化碳的平衡转化率为50%,则该反应条件下的平衡常数Kp= (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)![]() CH4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系:
CH4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系:

①该反应的ΔH 0(填“>”、“=”或“<”)。
②曲线c表示的物质为 。
③为提高H2的平衡转化率,除改变温度外,还可采取的措施是 ,用平衡移动原理说明理由 。
【答案】(1)-71.4kJ·mol-1
(2)①0.225mol·L-1·h-1②40%
(3)1/48MPa-2或0.0208MPa-2或0.021MPa-2
(4)①<②C2H4③加压(或不断分离出水)
【解析】
试题分析: (1)按顺序把热化学方程式标为①②③:
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3 kJ·mol-1 ①
CO(g)+1/2O2(g)=CO2(g) ΔH2= -283.0 kJ·mol-1 ②
H2(g)+1/2O2(g)=H2O(l) ΔH3= -285.8 kJ·mol-1 ③
根据盖斯定律,①×2-2×②-4×③得2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH=-71.4 kJ·mol-1。
(2)①由反应前后的压强关系可知2 h时,体系中气体的总的物质的量为3.4 mol,减少了0.6 mol。
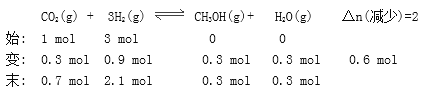
v(H2)=△c/△t=0.9mol/(2L*2h)=0.225 mol·L-1·h-1。②该反应是一个反应前后气体分子数减小的反应,压强不变时,说明反应达到平衡。5 h时反应达到平衡,根据反应前后压强的比值可求得CO2![]() 的平衡转化率为4mol*(1-0.8)/(2*1mol)×100%=40%。
的平衡转化率为4mol*(1-0.8)/(2*1mol)×100%=40%。
(3)设开始时投入CO2和H2的物质的量分别为1 mol和3 mol。

则平衡时p(CO2)=8 MPa×![]() =4/3 MPa,p(H2)=8 MPa×
=4/3 MPa,p(H2)=8 MPa×![]() =4 MPa,
=4 MPa,
p(CH3OH)=8 MPa×![]() =4/3 MPa,p(H2O)=8 MPa×
=4/3 MPa,p(H2O)=8 MPa×![]() =4/3 MPa,
=4/3 MPa,
Kp=![]() =
=![]() =
=![]() ≈0.020 8 (MPa-2)。(4)①由曲线变化可知随着温度升高,氢气的物质的量逐渐增多,说明升高温度平衡逆向移动,则正反应放热,ΔH<0。②随着温度升高,氢气的物质的量逐渐增多,因氢气为反应物,则另一条逐渐增多的曲线a代表CO2,由计量数关系可知曲线b代表水,曲线c代表C2H4。③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是增大压强或不断分离出水。
≈0.020 8 (MPa-2)。(4)①由曲线变化可知随着温度升高,氢气的物质的量逐渐增多,说明升高温度平衡逆向移动,则正反应放热,ΔH<0。②随着温度升高,氢气的物质的量逐渐增多,因氢气为反应物,则另一条逐渐增多的曲线a代表CO2,由计量数关系可知曲线b代表水,曲线c代表C2H4。③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是增大压强或不断分离出水。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】20世纪80年代后,人们发现和证实了一种新的含碳物质,它们是由一系列偶数个碳原子组成的分子,其中C60最具代表性。图中所示为n个C60连接而成的物质X 。下列有关说法不正确的是( )

A. X难溶于水,可以与氧气反应生成CO2
B. 该物质是一种新型的化合物
C. X是碳的一种同素异形体
D. X的摩尔质量为720ng·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是( )
酸 | 碱 | 盐 | |
A | H2SO4 | NaOH | BaCO3 |
B | H2S | K2CO3 | CuSO4 |
C | NaHSO4 | NaOH | CaCl2 |
D | HNO3 | KOH | Na2O |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在25℃、101 kPa下,1 6g甲醇(![]() )燃烧生成CO2和液态水时放热362.88 kJ。则表示甲醇燃烧热的热化学方程式为 。
)燃烧生成CO2和液态水时放热362.88 kJ。则表示甲醇燃烧热的热化学方程式为 。
(2)已知热化学方程式:SO2(g)+![]() O2(g)
O2(g)![]() SO3(g)△H=―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为 。
SO3(g)△H=―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向25 mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,滴定曲线如图所示,下列说法正确的是

A.在A、B间任一点的溶液中一定都有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.Ka(CH3COOH)=![]()
C.C点对应的溶液中,水电离出的H+浓度大于10-7 mol·L-1
D.D点对应的溶液中,存在如下关系:c(CH3COO-)-c(CH3COOH)=2c(H+)-c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是生产生活中用量最大的金属,B为淡黄色粉末。在常温下C为无色液体,E、G、H、I、J为气体,其中H为黄绿色,其它为无色.J能使湿润的红色石蕊试纸变蓝(图中部分产物已略去)。
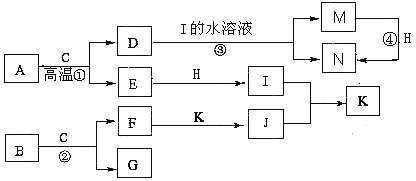
请填写下列空白
(1)写出化学式:M______,K______。
(2)写出①的化学方程式_________________________________;写出③的离子方程式_________________________________。
(3)反应④属于下列何种反应类型______(填字母序号)。
A.化合反应 B.氧化还原反应 C.离子反应 D.置换反应
(4)若要确定③反应后所得溶液中含有M物质,所选试剂为______(填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN C.浓氨水D.酸性高锰酸钾溶液
(5)常温下,H与过量的J反应产生浓厚的白烟,另一生成物是空气的主要成分之一,请写出该反应的化学方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向一个容积不变(1 L)的密闭容器中,加入3 mol PCl3和4 mol Cl2使之发生反应PCl3(g)+Cl2(g) ![]() PCl5(g),平衡时容器内压强为开始时的
PCl5(g),平衡时容器内压强为开始时的![]() 。
。
计算并回答:
(1)平衡时,容器内气体密度是开始时的___________倍,气体平均相对分子质量是开始时的_________倍。
(2)保持同一反应温度,若将起始物改为a mol PCl3,b mol Cl2,c mol PCl5。欲使平衡时PCl5的体积分数为![]() ,则a,b,c满足的关系为 , 。欲使开始时反应向逆方向进行,则a的取值范围为 , b的取值范围为 ,c的取值范围为
,则a,b,c满足的关系为 , 。欲使开始时反应向逆方向进行,则a的取值范围为 , b的取值范围为 ,c的取值范围为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.假说经过反复验证和修正,才发展成为科学的理论
B.模型一般可分为物体模型和思维模型
C.研究物质的性质常用观察、实验、分类、比较等方法
D.科学实验能解决化学学科的所有问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中,能表示反应X(g)+2Y(g)![]() 2Z(g),一定达到化学平衡状态的是( )
2Z(g),一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为1:2:2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y.
A.①② B.①④ C.②③ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com