
用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.1 mol N2所含有的原子数为NA
B.标准状况下,22.4 L水中含有的水分子数为NA
C.标准状况下,22.4 L氯化氢所含的原子数为NA
D.24 g O2和24 g O3所含的氧原子数都是1.5NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届河南省漯河市五校高一上学期期中联考化学试卷(解析版) 题型:选择题
在3NO2+H2O=2HNO3+NO中,氧化剂与还原剂的分子个数比为
A.2∶1 B.1∶2 C.3∶1 D.1∶3
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高一上学期期中考试化学试卷(A卷)(解析版) 题型:选择题
为了除去粗盐中的Ca2+、Mg2+、SO42―及泥沙,可将粗盐溶于水,然后进行下列五项操作,其中正确的操作顺序是( )
①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
A.①④②⑤③ B.④①②⑤③ C.④②①③⑤ D.⑤②④①③
查看答案和解析>>
科目:高中化学 来源:2016届河南省平顶山市高一第一学期期末调研考试化学试卷(解析版) 题型:填空题
在常见的非金属及其化合物中:
(1)晶体硅的导电性介于导体和绝缘体之间,是良好的 材料;硅酸钠水溶液俗称为 ,是制备硅胶和木材防火剂的原料;陶瓷、 、水泥等硅酸盐产品是使用量最大的无机非金属材料。
(2)氯元素是重要的“成盐元素”,将氯气通入NaOH溶液中可以得到漂白液,反应的离子方程式是 ;漂白液有效成分的化学式为 。
(3)水是常见的非金属元素化合物,请按要求写出下列水参加的反应的化学方程式。
①水只作氧化剂:
②NO2 气体通入水中:
③水既作氧化剂又作还原剂:
查看答案和解析>>
科目:高中化学 来源:2016届河南省平顶山市高一第一学期期末调研考试化学试卷(解析版) 题型:选择题
某同学对一无色透明溶液进行分析得出该溶液中含有下列某组离子,你认为该组离子应该是
A.Al3+、NO3―、K+、SO42ˉ B.Ca2+、H+、CO32ˉ、AlO2-
C.OHˉ、SO42ˉ、NH4+、Al3+ D.K+、Ca2+、HCO3-、OH-
查看答案和解析>>
科目:高中化学 来源:2016届河南省原名校高一上学期期末联考化学试卷(解析版) 题型:填空题
氯化铵简称“氯铵”,又称卤砂,为无色晶体或白色结晶性粉末,易溶于水中,在工农业生产中用途广泛。以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
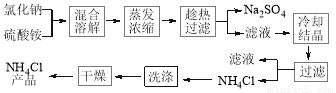
氯化铵和硫酸钠的溶解度随温度变化如图所示。回答下列问题:

(1)实验室进行蒸发浓缩用到的主要仪器有 、烧杯、玻璃棒、酒精灯等。
(2)实验过程中趁热过滤的目的是 。
(3)写出“蒸发浓缩”时发生的化学方程式: 。
(4)某研究性学习小组为测定该NH4Cl产品中氮的含量,设计了如图装置,并进行了讨论。
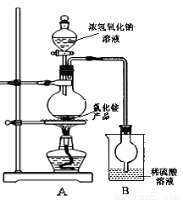
甲同学:根据此实验测得的数据,计算的NH4Cl产品的含氮量可能偏高,因为实验装置中存在一个明显缺陷是: ____ 。
乙同学:实验过程中,往烧瓶中加入的浓氢氧化钠溶液的离子反应方程式为 ,反应过程中NaOH一定要足量并充分加热,原因是 。
用改进后的实验装置重新进行实验,称取13.0gNH4Cl产品,测得实验后B装置增重3.4g。则该化肥含氮量为 。
查看答案和解析>>
科目:高中化学 来源:2016届河南省原名校高一上学期期末联考化学试卷(解析版) 题型:选择题
将3.9 g镁铝合金,投入到500 mL 2 mol/L的盐酸中,合金完全溶解,再加入5 mol/L的NaOH溶液,若要生成的沉淀最多,加入的这种NaOH溶液的体积是
A.100 mL B.150 mL C.200 mL D.250 mL
查看答案和解析>>
科目:高中化学 来源:2016届河北省高一下学期第一次月考化学试卷(解析版) 题型:选择题
按要求写出下列反应的化学方程式
(1)短周期元素组成的三种有色物质(单质或化合物)可以与水发生氧化还原反应,水既不是氧化剂也不是还原剂,按相对分子质量由小到大的顺序写出三种物质与水反应的方程式。
①
②
③
(2)由短周期元素构成的两种单质与水发生氧化还原反应
④水只作氧化剂
⑤水只作还原剂
查看答案和解析>>
科目:高中化学 来源:2016届河北冀州中学高一上学期第四次月考化学试卷(解析版) 题型:选择题
把a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为( )
A.70% B.52.4% C.47.6% D.30%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com