
ВИ»Їп§јтіЖЎ°ВИп§Ў±Ј¬УЦіЖВ±Й°Ј¬ОЄОЮЙ«ѕ§Ме»т°ЧЙ«Ѕбѕ§РФ·ЫД©Ј¬ТЧИЬУЪЛ®ЦРЈ¬ФЪ№¤Е©ТµЙъІъЦРУГНѕ№г·єЎЈТФВИ»ЇДЖєНБтЛбп§ОЄФБПЦЖ±ёВИ»Їп§ј°ё±ІъЖ·БтЛбДЖЈ¬№¤ТХБчіМИзПВЈє
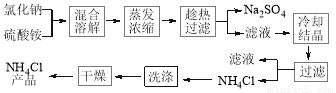
ВИ»Їп§єНБтЛбДЖµДИЬЅв¶ИЛжОВ¶И±д»ЇИзНјЛщКѕЎЈ»ШґрПВБРОКМвЈє

ЈЁ1Ј©КµСйКТЅшРРХф·ўЕЁЛхУГµЅµДЦчТЄТЗЖчУР ЎўЙХ±ЎўІЈБ§°фЎўѕЖѕ«µЖµИЎЈ
ЈЁ2Ј©КµСй№эіМЦРіГИИ№эВЛµДДїµДКЗ ЎЈ
ЈЁ3Ј©РґіцЎ°Хф·ўЕЁЛхЎ±К±·ўЙъµД»ЇС§·ЅіМКЅЈє ЎЈ
ЈЁ4Ј©ДіСРѕїРФС§П°РЎЧйОЄІв¶ЁёГNH4ClІъЖ·ЦРµЄµДє¬БїЈ¬ЙијЖБЛИзНјЧ°ЦГЈ¬ІўЅшРРБЛМЦВЫЎЈ
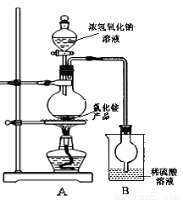
јЧН¬С§ЈєёщѕЭґЛКµСйІвµГµДКэѕЭЈ¬јЖЛгµДNH4ClІъЖ·µДє¬µЄБїїЙДЬЖ«ёЯЈ¬ТтОЄКµСйЧ°ЦГЦРґжФЪТ»ёцГчПФИ±ПЭКЗЈє ____ ЎЈ
ТТН¬С§ЈєКµСй№эіМЦРЈ¬НщЙХЖїЦРјУИлµДЕЁЗвСх»ЇДЖИЬТєµДАлЧУ·ґУ¦·ЅіМКЅОЄ Ј¬·ґУ¦№эіМЦРNaOHТ»¶ЁТЄЧгБїІўід·ЦјУИИЈ¬ФТтКЗ ЎЈ
УГёДЅшєуµДКµСйЧ°ЦГЦШРВЅшРРКµСйЈ¬іЖИЎ13.0gNH4ClІъЖ·Ј¬ІвµГКµСйєуBЧ°ЦГФцЦШ3.4gЎЈФтёГ»Ї·Кє¬µЄБїОЄ ЎЈ
ЈЁ1Ј©Хф·ўГу
ЈЁ2Ј©·АЦ№ВИ»Їп§ѕ§МеОціц¶шЛрєД
ЈЁ3Ј©ЈЁNH4Ј©2SO4Ј«2NaCl= Na2SO4ЎэЈ«2NH4Cl
ЈЁ4Ј©ўЩAЎўBЧ°ЦГјдИ±Т»ёцёЙФпЧ°ЦГ ўЪ NH4++OH- NH3Ўь+H2O
NH3Ўь+H2O
К№ВИ»Їп§ід·Ц·ґУ¦НкИ«ЧЄ»ЇОЄNH3 21.5ЈҐ
ЎѕЅвОцЎї
КФМв·ЦОцЈєЈЁ1Ј©КµСйКТЅшРРХф·ўЕЁЛхУГµЅµДЦчТЄТЗЖчУРХф·ўГуЎўЙХ±ЎўІЈБ§°фЎўѕЖѕ«µЖµИЈ¬
ЈЁ2Ј©УЙНјПсїЙТФїґіцЈ¬ФЪДіТ»ОВ¶И·¶О§ДЪЈ¬ВИ»Їп§µДИЬЅв¶ИµНУЪБтЛб淋ДИЬЅв¶ИЈ¬ЛщТФіГИИ№эВЛ·АЦ№ВИ»Їп§ѕ§МеОціц¶шЛрєДЈ¬їЙТФК№БтЛбп§ТФіБµнРОКЅВЛіц¶шВИ»Їп§БфФЪВЛТєАпЎЈ
ЈЁ3Ј©Хф·ўЕЁЛхК±БтЛбп§ТФ№ММеРОКЅґжФЪЈ¬ЛщТФ»ЇС§·ЅіМКЅОЄЈЁNH4Ј©2SO4Ј«2NaCl= Na2SO4ЎэЈ«2NH4Cl
 ЈЁ4Ј©ўЩ°±ЖшФЪЅшИлBЦ®З°ОґёЙФпЈ¬ЛщТФє¬µЄБїЖ«ёЯЈ¬У¦ФЪAЎўBЧ°ЦГјдјУТ»ёцёЙФпЧ°ЦГЈ¬
ЈЁ4Ј©ўЩ°±ЖшФЪЅшИлBЦ®З°ОґёЙФпЈ¬ЛщТФє¬µЄБїЖ«ёЯЈ¬У¦ФЪAЎўBЧ°ЦГјдјУТ»ёцёЙФпЧ°ЦГЈ¬
ўЪЙХЖїЦР·ўЙъµДАлЧУ·ЅіМКЅКЗЗїјоУлп§СОИЬТєµД·ґУ¦Ј¬АлЧУ·ЅіМКЅОЄNH4++OH-= NH3Ўь+H2OЈ»јоТЄЧгБїµДДїµДѕНКЗК№п§ёщАлЧУИ«ІїЧЄ»ЇОЄ°±ЖшЈ»3.4gјґОЄ°±ЖшµДЦКБїЈ¬ЖдµЄФЄЛШµДЦКБїОЄ3.4gЎБ14ЎВ17=2.8g,ЛщТФє¬µЄБїОЄ2.8g/13.0gЎБ100%=21.5%ЎЈ
їјµгЈєїјІй»ЇС§У빤ҵЙъІъµДБЄПµЎў¶ФКµСйµД·ЦОцЎўКµСйЧ°ЦГµДЕР¶ПЈ¬АлЧУ·ЅіМКЅµДКйРґЎў»ЇС§јЖЛгµИ


 іцІКН¬ІЅґуКФѕнПµБРґр°ё
іцІКН¬ІЅґуКФѕнПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2016ЅмєУДПКЎдрєУКРОеРЈёЯТ»ЙПС§ЖЪЖЪЦРБЄїј»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРОпЦКЛ®ИЬТєДЬµјµзЈ¬µ«ёГОпЦККфУЪ·ЗµзЅвЦКµДКЗ
AЈ®Na2O BЈ®Cl2 CЈ®H2SO4 DЈ®SO2
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2016ЅмєУДПКЎВеСфКРёЯТ»ЙПС§ЖЪЖЪЦРїјКФ»ЇС§КФѕнЈЁAѕнЈ©ЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБР·ґУ¦¶јУРЛ®ІОјУЈ¬ЖдЦРКфУЪСх»Ї»№Ф·ґУ¦Ј¬¶шЛ®јИІ»ЧцСх»ЇјБЈ¬УЦІ»Чц»№ФјБµДКЗ
AЈ®2F2+2H2O=4HF+O2 BЈ®2Na+2H2O=2NaOH+H2Ўь
CЈ®C12+H2O=HC1O+HC1 DЈ®C+H2O CO+H2
CO+H2
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2016ЅмєУДПКЎЖЅ¶ҐЙЅКРёЯТ»µЪТ»С§ЖЪЖЪД©µчСРїјКФ»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРКФјБЦРЈ¬І»ДЬУГУЪјш±рFe2+єНFe3+µДКЗ
AЈ®NaOHИЬТє BЈ®ПЎБтЛб
CЈ®KSCNИЬТє DЈ®ЛбРФKMnO4ИЬТє
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2016ЅмєУДПКЎЖЅ¶ҐЙЅКРёЯТ»µЪТ»С§ЖЪЖЪД©µчСРїјКФ»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
УГNA±нКѕ°ў·ьјУµВВЮіЈКэµДЦµЈ¬ПВБРЛµ·ЁЦРХэИ·µДКЗ
AЈ®1 mol N2Лщє¬УРµДФЧУКэОЄNA
BЈ®±кЧјЧґїцПВЈ¬22.4 LЛ®ЦРє¬УРµДЛ®·ЦЧУКэОЄNA
CЈ®±кЧјЧґїцПВЈ¬22.4 LВИ»ЇЗвЛщє¬µДФЧУКэОЄNA
DЈ®24 g O2єН24 g O3Лщє¬µДСхФЧУКэ¶јКЗ1.5NA
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2016ЅмєУДПКЎФГыРЈёЯТ»ЙПС§ЖЪЖЪД©БЄїј»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
Ѕ«2.5g Na2CO3ЎўNaHCO3ЎўNaOHµД№ММе»мєПОпНкИ«ИЬЅвУЪЛ®Ј¬ЦЖіЙИЬТєЈ¬И»єуПтёГИЬТєЦРЦрµОјУИл1 mol/LµДСОЛбЈ¬ЛщјУСОЛбµДМе»эУлІъЙъCO2µДМе»эЈЁ±кЧјЧґїцЈ©№ШПµИзПВНјЛщКѕЈ¬ПВБРЛµ·ЁЦРґнОуµДКЗ
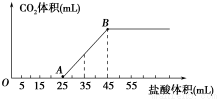
AЈ®OA¶О·ўЙъ·ґУ¦µДАлЧУ·ЅіМКЅОЄHЈ«Ј«OHЈ=H2O CO32-Ј«HЈ«=HCO3-
BЈ®AµгИЬТєЦРµДИЬЦКОЄNaC1ЎўNaHCO3
CЈ®»мєПОпЦРNaOHµДЦКБї0.6g
DЈ®µ±јУИл35mLСОЛбК±Ј¬ІъЙъCO2µДМе»эОЄ336mL
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2016ЅмєУДПКЎФГыРЈёЯТ»ЙПС§ЖЪЖЪД©БЄїј»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРПЦПу»тРФЦКДЬМеПЦДЖµДОпАнРФЦКµДКЗ
ўЩДЖИјЙХК±·ўіц»ЖЙ«µД»рСж ўЪДЖИјЙХК±ЙъіЙ№эСх»ЇДЖ ўЫИЫµгµН ўЬГЬ¶И±ИЛ®ўЭИИєНµзµДБјµјМе ўЮДЖУРєЬЗїµД»№ФРФ
AЈ®ўЩўЫўЬўЭўЮЎЎЎЎЎЎ BЈ®ўЩўЪўЫўЬўЭЎЎ CЈ®ўЪўЫўЬўЭ DЈ® ўЩўЫўЬўЭ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2016ЅмєУ±±КЎёЯТ»ПВС§ЖЪµЪТ»ґОФВїј»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
FeєНFe2O3 µД»мєПОп№І13Ј®6gЈ¬јУИл150mLПЎH2SO4Ј¬ФЪ±кЧјЧґїцПВКХјЇµЅ1Ј®12LH2Ј¬FeєНFe2O3 ѕщОЮКЈУаЎЈОЄЦРєН№эБїµДH2SO4Ј¬ІўК№FeSO4 И«ІїЧЄ»ЇОЄFe(OH)2 іБµнЈ¬ПыєДБЛ200mL 3mol/LµДNaOHИЬТєЈ¬ФтёГH2SO4 µДОпЦКµДБїЕЁ¶ИОЄ
AЈ®2Ј®25mol/L BЈ®2mol/L CЈ®0Ј®3mol/L DЈ®0Ј®6mol/L
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2016ЅмєУ±±јЅЦЭЦРС§ёЯТ»ЙПС§ЖЪµЪЛДґОФВїј»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
іЈОВПВЈ¬НщH2O2ИЬТєЦРµОјУЙЩБїFeSO4ИЬТєЈ¬їЙ·ўЙъИзПВБЅёц·ґУ¦Јє
2Fe2Ј«Ј«H2O2Ј«2HЈ«=2Fe3Ј«Ј«2H2O 2Fe3Ј«Ј«H2O2=2Fe2Ј«Ј«O2ЎьЈ«2HЈ«
ПВБРЛµ·ЁІ»ХэИ·µДКЗЈЁЎЎЎЎЈ©
AЈ®H2O2µДСх»ЇРФ±ИFe3Ј«ЗїЈ¬Жд»№ФРФ±ИFe2Ј«Их
BЈ®ФЪ·ґУ¦№эіМЦРЈ¬ИЬТєµДpH»щ±ѕІ»±д
CЈ®ФЪ·ґУ¦№эіМЦРЈ¬Fe2Ј«єНFe3Ј«µДЧЬБї±ЈіЦІ»±д
DЈ®H2O2ЙъІъ№эіМТЄСПёс±ЬГв»мИлFe2Ј«
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com