
��16�֣�
CuCl��Ӧ�ù㷺���л��ϳɴ������ɲ�ȡ��ͬ������ȡ��
����һ ͭ�ۻ�ԭCuSO4��Һ

��֪��CuCl������ˮ���Ҵ�����ˮ��Һ�д���ƽ�⣺CuCl(��ɫ)+ 2Cl��  [CuCl3]2��(��ɫ��Һ)��
[CuCl3]2��(��ɫ��Һ)��
��1������ͭ������ȵ�H2SO4��Һ�У���ͨ���������������CuSO4���÷�Ӧ�����ӷ���ʽΪ ��
��2�����У������ȡ���Ŀ���� �����۲쵽 ����������Ӧ�Ѿ���ȫ��
��3�����У��������ˮ�������� ��
��4����ʪ��CuCl�ڿ���������ˮ������������������У�Ϊ��ֹˮ������������ӵ��Լ����ȡ�IJ����� ��
������ ͭ�缫��ⱥ��ʳ��ˮ��ʵ��װ����ͼ��

��5�������ĵ缫��ӦʽΪ ��
��6��ʵ�鿪ʼʱ����������û�в���CuOH������ԭ���� ������֪��Ksp(CuCl)=1.2��10-6��Ksp(CuOH)=1.2��10-14��
��15�֣�
��1��2Cu+O2+4H+ 2Cu2++ 2H2O
2Cu2++ 2H2O
��2���ӿ췴Ӧ������ ��Һ����ɫ��Ϊ��ɫ
��3��ϡ�ʹٽ�ƽ��CuCl(��ɫ)+ 2Cl��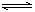 [CuCl3]2��(��ɫ��Һ)�����ƶ�������CuCl��
[CuCl3]2��(��ɫ��Һ)�����ƶ�������CuCl��
��4��Ũ���ᡢ95%�Ҵ�����ո���
��5��Cu - e��+ Cl��= CuCl��дCu - e��+ 3Cl��= [CuCl3]2��Ҳ���� ��
��6��������Cl-Ũ��ԶԶ����OH-��Ũ��
��������
�����������1������ͭ������ȵ�H2SO4��Һ�У���ͨ���������������CuSO4��˵��ͭ�������Լ����ᷴӦ��������ͭ��ˮ����Ӧ�����ӷ���ʽΪ2Cu+O2+4H+ 2Cu2++ 2H2O��
2Cu2++ 2H2O��
��2�������¶��ܼӿ컯ѧ��Ӧ���ʣ����С����ȡ���Ŀ���Ǽӿ췴Ӧ�����ʣ�����ͭ��Һ����NaCl������ͭ�ۡ�Ũ��������[CuCl3]2��(��ɫ��Һ)�����Ե��۲쵽��Һ����ɫ��Ϊ��ɫ����������Ӧ�Ѿ���ȫ��
��3�����м������ˮ��CuCl(��ɫ)+ 2Cl��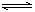 [CuCl3]2��(��ɫ��Һ)����ˮϡ�ͣ�ƽ�������ƶ�����CuCl��ɫ������
[CuCl3]2��(��ɫ��Һ)����ˮϡ�ͣ�ƽ�������ƶ�����CuCl��ɫ������
(4) ��ʪ��CuCl�ڿ���������ˮ�������,����Ũ����������ˮ�⣬CuCl������ˮ���Ҵ��������Ҵ��ܷ�ֹ�������������������У�Ϊ��ֹˮ������������ӵ��Լ����ȡ�IJ�����Ũ���ᡢ95%�Ҵ�����ո��
��5��ͭ�ǻ��Ե缫����ͭ���缫��ͭ�������������ĵ缫��ӦʽΪCu - e��+ Cl��= CuCl��
��6��ʵ�鿪ʼʱ��������Cl-Ũ��ԶԶ����OH-��Ũ�ȣ�������������û�в���CuOH������
���㣺����ͭ���仯��������ʣ�����Ӧ�õ�֪ʶ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ����3�½β������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�H3PO4��NaOH��Һ��Ӧ����ϵ�У��������ֵķֲ�����(ƽ��ʱij���ֵ�Ũ��ռ������Ũ��֮�͵ķ���)��pH �Ĺ�ϵ����ͼ��ʾ[��֪Ca3(PO4)2������ˮ]�������й�˵������ȷ����

A��H3PO4��Ka3=10-12.2��HPO42-��ˮ��ƽ�ⳣ��Ϊ10-6.8
B��Na2HPO4 ��Һ�Լ��ԣ�������Һ�м���������CaCl2 ��Һ����Һ��������
C��Ϊ��þ����ܴ���NaH2PO4��pHӦ������4��5.5����
D�� pH=13ʱ����Һ�и���Ũ�ȴ�С��ϵΪ��c(Na+)��c(HPO42-)��c(PO43��)��c(OH��)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ������ѧ�ڵ�һ���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ����ᡢ���������������ء�����˵����ȷ����
A������ľ�ĵ���Ҫ�ɷֶ�����ά�أ���˿������˿����Ҫ�ɷֶ��ǵ�����
B��ʯ����ɵõ�ʯ���������͡�ú�͡����͵�
C���Ӻ�ˮ����ȡ���ʶ�����ͨ����ѧ��Ӧ����ʵ��
D�����������������ͨ�������ճ�������Ҳ���ô�����Һ����ȥ��Ʒ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�������������ۻ�ѧ�Ծ��������棩 ���ͣ������
(15��)ͭ���仯�����������������ϵ���С�
��1��������Cu(OH)2�������Ƿ�Ӧ�Ʊ�Cu2O���÷�Ӧ���������� (�����������ԭ����)
��2����H2O2ϡ���Ṳͬ���ݷ�ӡˢ��·����Ʊ�CuSO4�����÷�Ӧ��Ƴ�ԭ��أ�
�����ĵ缫��ӦʽΪ
��3����NH4NO3��������ͭ(��Cu��CuO)����CuCl�IJ�����������:
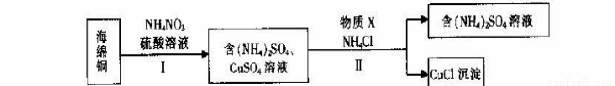
�ٲ���I�У���Ӧ�¶Ȳ��˹��ߵ�ԭ���� ��
�ڲ���I�У�0��5 mol NH4NO3�μӷ�Ӧ��4mol����ת�ƣ�ͭ���뷴Ӧ�����ӷ���ʽΪ ��
�۲���II�У�����X��ѡ�õ������� ��(�����)��
a��Cu b��C12 c��H2O2 d��(NH4)2SO3
�ܲ���II������X��Ҫ������ԭ����һ�Ǽӿ췴Ӧ���ʣ������ _��
�ݲ���II�е�NH4 Cl�ӵ�һ������ʱ������CuCl �Ჿ���ܽ�����CuCl2-��һ���¶��½�������ƽ��:
Cu Cl(s) 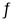 Cu+(a q) + Cl-(a q) Ksp=1��4x10-6
Cu+(a q) + Cl-(a q) Ksp=1��4x10-6
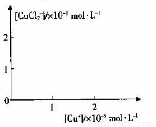
Cu Cl(s) + Clһ(a q) CuCl2(a q) K=0��35
CuCl2(a q) K=0��35
����[Cu+]��[CuCl2-]��Ksp,K����ѧ��ϵ����ͼ�л�����Cu+]��[CuCl2]-�Ĺ�ϵ����(Ҫ�����ٱ�������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�������������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A���Ҵ��Ͷ��ȼ��鶼����ͬ���칹��
B��֬�ڼ��������²���ˮ��
C���ƾ���ϩ���ϵķ�Ӧ����ȡ����Ӧ
D���������������õ����ʱ��Ե�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡȪ���и���3�½�ѧ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�Ũ�Ⱦ�Ϊ1.0 mol��L-1��NH3��H2O��NH4Cl�����Һ10 mL�������pHΪ9.3������
�й�������ȷ����
A������������NaCl����ʹc(NH4+) = c(Cl-)
B���μӼ���Ũ��ˮ��c(NH4+)��С
C���μӼ���Ũ���ᣬ ��ֵ��С
��ֵ��С
D��1.0 mol��L-1��NH4Cl��Һ��c(NH4+)�ȸû����Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�����ѧ����������ۻ�ѧ�Ծ� �������棩 ���ͣ������
��14�֣�Al2O3��Al(OH)3������Ҫ����ԭ�ϡ�����Ҫ��ش����⣺
��ⷨ�Ƹ�Ʒ��Al(OH)3װ�����£��м������ӽ���Ĥ��������
4Na[Al(OH)4]+2H2O 4Al(OH)3��+4NaOH+O2��+2H2��
4Al(OH)3��+4NaOH+O2��+2H2��

��1������Al(OH)3�� ���������������������������
��2�������ת��2mol e��ʱ�����Ƶ�__________mol��Al(OH)3��
����ȡ����Al2O3��Ҫ������������������0.05mol��L-1��������Һ������⣬����Fe2+��Fe3+���ɰ����������ᴿ������Һ�м�����H2O2��ַ�Ӧ�������Լ�X������ҺpH=3.5���������£�0.1mol��L-1��Fe2+��Al3+��ʼ������pH�ֱ�Ϊ7.0��3.7��Fe3+��ȫ������pH=3.2��
��3��������������ɢ�ڷ�ɢ���н��γɽ��塣��������������ֱ��ԼΪ_________m��
��4��������������Һ����Fe3+ʱ�������õ��Լ���������_____________________��
��5������Һ�м���H2O2�������� �������ӷ���ʽ��ʾ����
��6�������X�Լ�����ѡ���ţ��� ��
A��CuO B��Al(OH)3 C��NaOH D��NaHCO3
�����ں���Һ��pHƫ��3.5�����ܴ����ĺ����__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ��������ɽ����ѧ�ڸ�һ��ѧ��ĩ�Ծ��������棩 ���ͣ�ѡ����
ͬ��ͬѹ�£���������SO2��CO2��Ƚϣ�����������ȷ����
A�������Ϊ11�U16 B���ܶȱ�Ϊ11�U16
C����ԭ������Ϊ1�U1 D�����ʵ�����Ϊ16�U11
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��X����ͨ��BaCl2��Һ��δ���������ɣ�Ȼ��ͨ��Y���壬�г������ɣ�X��Y��������
ѡ�� | X | Y |
A | SO2 | H2S |
B | Cl2 | CO2 |
C | NH3 | CO2 |
D | SO2 | Cl2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com