
【题目】同种元素的不同微粒,它们的:
A. 核外电子数一定相等B. 中子数一定相等
C. 质子数一定相等D. 化学性质不一定相同
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】(多选)如图所示的实验,不能达到实验目的是( )
A | B | C | D |
|
|
|
|
证明温度对平衡移动的影响验证 | 实现了化学能与电能相互转化 | 验证铁钉发生吸氧腐蚀 | 制备少量的氧气 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( ) 
A.图①表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2(g)+O2(g)2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 molL﹣1 KMnO4 酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸铵广泛应用与工农生产中,其生产流程图如下,回答下列问题: 
(1)在上述工业制硝酸的生产中,B设备的名称是 , 在反应中的氧化产物是 .
(2)此生产过程中,N2与H2合成NH3所用的催化剂是 . 在合成氨的设备(合成塔)中,设置热交换器的目的是;在合成硝酸的吸收塔中通入空气的目的是 .
(3)科学家以氨(NH3)为燃料开发新型的燃料电池.电池中填充可传导O2﹣离子的 MnO3固体电解质,电池总反应为:4NH3+3O2=2N2+6H2O.负极的电极反应式为 .
(4)某化肥厂用NH3制备NH4NO3 . 已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量约占总耗NH3质量(不考虑其它损耗)的%.(取两位有效数字)
(5)硝酸铵是一种常用的氮肥,在使用该化肥时避免与碱性肥料一起使用,理由是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是:
A. 由H原子形成1 molH-H键要吸收热量B. 所有燃烧反应都是放热反应
C. 有的化学反应没有能量变化D. 凡经加热而发生的化学反应都是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法不正确的是( ) 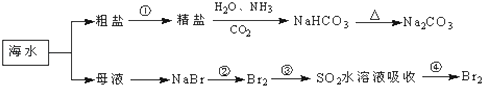
A.工业上通过电解熔融状态MgCl2制取金属镁
B.用澄清的石灰水可鉴别NaHCO3和Na2CO3
C.在第②、④步骤中,溴元素均被氧化
D.制取NaHCO3的反应是利用其溶解度小于NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①Cl2+2KBr=2KCl+Br2 , ②KClO3+6HCl=3Cl2+KCl+3H2O,③2KBrO3+Cl2=Br2+2KClO3 , 下列说法正确的是( )
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C.反应②中还原剂与氧化剂的物质的量之比为6:1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图1装置制取氯气,并用氯气进行实验.回答下列问题: 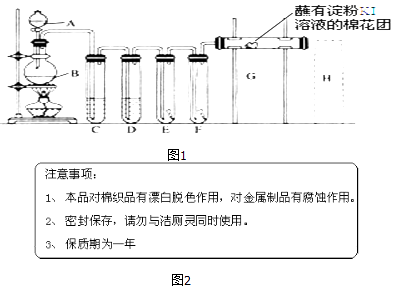
(1)A中盛有浓盐酸,B中盛有MnO2 , 写出反应的化学方程式 .
(2)D中放入浓H2SO4 , 其目的是 .
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是: , 对比E和F中现象的差异可得出的结论及解释是 .
(4)G处的现象是 .
(5)画出H处尾气吸收装置图并注明试剂 .
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生.某品牌消毒液包装上说明如图2. ①“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式: .
②需“密闭保存”的原因;
③分析“对金属制品有腐蚀作用”的原因可能是;
(7)现在有一种名为“净水丸”的产品也能对饮用水进行快速的杀菌消毒,药丸通常分内外两层.外层的优氯净 Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去. ①亚硫酸钠将水中多余次氯酸除去的离子反应方程式为 .
②亚硫酸钠溶液在空气中易变质,请完整写出检验亚硫酸钠溶液是否变质的实验操作方案 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com