
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )

A. 溶液中一定不含CO32﹣,可能含有SO42-和NO3-
B. 溶液中n(NH4+)="0.2" mol
C. 溶液中的阳离子只有H+、Mg2+、Al3+
D. n(H+)︰n(Al3+)︰n(Mg2+)=1︰1︰1
【答案】B
【解析】试题分析:A、加锌产生无色无味气体说明锌与氢离子反应生成氢气,溶液中有大量氢离子,则没有碳酸根和硝酸根离子,因为硝酸根、氢离子与锌会反应生成刺激性的一氧化氮,A错误;B、根据图象特点可以知道:加入氢氧化钠,先与氢离子反应,再与镁、铝离子反应生成氢氧化物沉淀,再与铵根反应得到一水合氨,再与氢氧化铝反应生成偏铝酸钠,根据第二段是氢氧化钠与铵根反应得到一水合氨的阶段,即NH4++OH-=NH3H2O,消耗氢氧化钠的物质的量为0.7mol-0.5mol=0.2mol,所以溶液中n(NH4+)=0.2mol,B正确;C、据图象特点可以知道:加入氢氧化钠,先与氢离子反应,再与镁、铝离子反应生成氢氧化物沉淀,再与铵根反应得到一水合氨,再与氢氧化铝反应生成偏铝酸钠,所以溶液中的阳离子一定含NH4+、H+、Mg2+、Al3+,C错误;D、根据第一段是氢氧化钠中和氢离子的阶段,所以氢离子的物质的量是0.1mol,根据第四段是氢氧化铝和氢氧化钠反应的阶段,即Al(OH)3~OH-~[Al(OH)4]-,则消耗氢氧化钠的物质的量为:0.8mol-0.7mol=0.1mol,根据第二段是将铝离子和镁离子反应生成沉淀的阶段,根据Al3+~3OH-~Al(OH)3,Mg2+~2OH-~Mg(OH)2,0.1mol氢氧化铝消耗氢氧化钠的物质的量是0.3mol,所以镁离子消耗氢氧化钠的物质的量是:0.5mol-0.1mol-0.3mol=0.1mol,所以镁离子的物质的量是0.05mol,即n(H+)︰n(Al3+)︰n(Mg2+)=0.1:0.1:0.05=2:2:1,D错误,答案选B。
【考点定位点评】本题是一道关于离子反应和离子检验知识的题目
【名师点晴】该题难度较大,侧重于考查学生分析和解决问题的能力,明确常见离子的性质和根据图像曲线判断出反应的化学方程式为解答的关键。关于图像的答题需要注意以下几点:①看面:弄清纵、横坐标的含义。②看线:弄清线的变化趋势,每条线都代表着一定的化学反应过程。③看点:弄清曲线上拐点的含义,如与坐标轴的交点、曲线的交点、折点、最高点与最低点等。曲线的拐点代表着一个反应过程的结束和开始。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃,向50mL 0.018mol/L AgNO3溶液中加入50mL 0.02mol/L 盐酸生成沉淀.已知:Ksp(AgCl)=1.8×10﹣10 , 则生成沉淀后的体系中c(Ag+)为( )
A.1.8×10﹣7mol/L
B.1.8×10﹣8 mol/L
C.1.8×10﹣9mol/L
D.1.8×10﹣10mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时,Ksp(NiS)=1.0×10-21,Ksp(FeS)=6.0× 10-18,其沉淀溶解平衡曲线如图所示(图中R表示Ni或Fe),下列说法正确的是(已知: ![]() ≈2.4,
≈2.4, ![]() ≈3.2) ( )
≈3.2) ( )
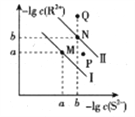
A. M点对应的溶液中,c(S2-)≈3.2×10-11 mol·L-1
B. 与P点相对应的NiS的分散系是均一稳定的
C. 向Q点对应的溶液中加水,可转化成N点对应的溶液
D. FeS+Ni2+![]() NiS+Fe2+的平衡常数K=6000
NiS+Fe2+的平衡常数K=6000
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定浓度的下列溶液,不外加任何试剂就能依次鉴别出来,正确的鉴别顺序为( ) ①NaOH溶液②(NH4)2SO4溶液③BaCl2溶液④KNO3溶液⑤FeCl3溶液.
A.①②③④⑤
B.②③⑤④①
C.⑤①②③④
D.⑤③②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,可逆反应C(s)+CO2(g)![]() 2CO(g),达到平衡状态的标志是( )
2CO(g),达到平衡状态的标志是( )
①单位时间内生成n molCO2的同时生成n molC ②单位时间内生成n molCO2 的同时生成2n mol CO ③CO2 、CO的物质的量浓度之比为1: 2的状态 ④混合气体的密度不再改变的状态 ⑤混合气体的压强不再改变的状态 ⑥C的质量不再改变的状态
A. ①④⑤⑥ B. ②④⑤⑥ C. ②③⑤⑥ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列图示的说法中正确的是( )
A.由图①所示实验可得出三种元素的非金属性强弱顺序是:氯>碳>硅
B.图②可用于干燥、收集氯化氢,并吸收多余的氯化氢
C.图③表示可逆反应CO(g)+H2O(g)CO2(g)+H2(g)的△H>0
D.对反应:A(s)+2B(g)xC(g),根据图④可以求出x=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂。某兴趣小组用如图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去)。

查阅资料可知:
①2NO+Na2O2=2NaNO2;2NO2+Na2O2 =2NaNO3。
②NO能被酸性KMnO4氧化成NO3-。
(1)装置中仪器a的名称为____________。A中反应的化学方程式_____________。
(2)装置B中观察到的主要现象______________。
(3)装置C中盛放的试剂是______________。
(4)装置E的作用是______________。
(5)A中滴入浓硝酸之前,应先通入N2一段时间,原因是____________。
(6)写出NO被酸性KMnO4氧化的离子反应方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如下图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | A中的物质 | B中的物质 | C中收集的气体 | D中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com