
【题目】在固定容积的密闭容器中,有可逆反应nA(g)+mB(g)pC(g)处于平衡状态(已知n+m>p,△H>0).升高温度时 ![]() 的比值;加入催化剂,气体的总物质的量;充入C,则A、B的物质的量 . (增大、减小、不变、不确定)
的比值;加入催化剂,气体的总物质的量;充入C,则A、B的物质的量 . (增大、减小、不变、不确定)
【答案】减小;不变;增大
【解析】解:△H>0,说明正反应吸热,升高温度,平衡向正反应方向移动,则 ![]() 的比值减小,加入催化剂,平衡不移动,则气体的总物质的量不变,充入C,平衡逆向移动,A、B的物质的量增大,所以答案是:减小;不变;增大.
的比值减小,加入催化剂,平衡不移动,则气体的总物质的量不变,充入C,平衡逆向移动,A、B的物质的量增大,所以答案是:减小;不变;增大.
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)).


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某强碱性溶液中含有的离子是K+、NH4+、Al3+、AlO2﹣、CO32﹣、SiO32﹣、Cl﹣中的某几种,现进行如下实验: ①取少量的溶液用硝酸酸化后,该溶液无沉淀生成;
②另取一定量原溶液,逐滴加入盐酸至过量,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
③另取一定量的原溶液中加入5mL0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g.
下列说法中正确的是( )
A.该溶液中一定不含NH4+、Al3+、SiO32﹣、Cl﹣
B.该溶液中一定含有Al3+、CO32﹣、Cl﹣
C.Cl﹣可能含有
D.该溶液中一定含有AlO2﹣、CO32﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
电离能 I1 I2 I3 I4 … |
In/kJ.mol﹣1 578 1817 2745 11578 … |
则该元素是(填写元素符号).
(2)基态锗(Ge)原子的电子排布式是 . Ge的最高价氯化物分子式是 . 该元素可能的性质或应用有 .
A.是一种活泼的金属元素 B.其电负性大于硫 C.其单质可作为半导体材料 D.其最高价氯化物的沸点低于其溴化物的沸点
(3)关于化合物 ![]() , 下列叙述正确的有 .
, 下列叙述正确的有 .
A.分子间可形成氢键
B.分子中既有极性键又有非极性键
C.分子中有7个σ键和1个π键
D.该分子在水中的溶解度大于2﹣丁烯
(4)NaF的熔点  的熔点(填>、=或<),其原因是 .
的熔点(填>、=或<),其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法正确的是
A.使用漂白液时不可与酸性洁厕剂混用
B.淘米水中含有淀粉可以直接检测加碘盐中是否含有碘元素
C.葡萄糖、油脂、蛋白质等进入人体内经水解后被吸收
D.铝壶表面有致密氧化膜耐腐蚀,可长期存放食醋
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.燃料电池由外设装备提供燃料和氧化剂
B.Mg和Al通常用热还原的方法来冶炼
C.绿色化学的核心是应用化学原理对环境污染进行治理
D.蛋白质、棉花、淀粉、油脂都是由高分子组成的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成: 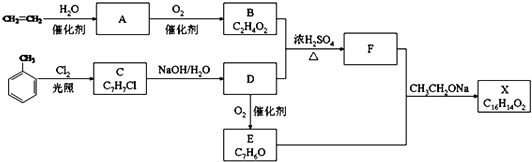
已知:RCHO+CH3COOR′ ![]() RCH=CHCOOR′请回答:
RCH=CHCOOR′请回答:
(1)A中官能团的名称是;C→D的反应类型为;
(2)B+D→F的化学方程式;
(3)E的结构简式;
(4)对于化合物X,下列说法正确的是;
A.能发生水解反应
B.能发生银镜反应
C.不与浓硝酸发生取代反应
D.能使Br2的CCl4溶液褪色
(5)F有多种同分异构体,含有酯基和一取代苯结构的同分异构体有五个,其中四个的结构简式是: ![]() CH2CH2OOCH、
CH2CH2OOCH、 ![]() COOCH2CH3、
COOCH2CH3、 ![]() CH2COOCH3、
CH2COOCH3、 ![]() 00CCH2CH3 . 请写出另外一个同分异构体的结构简式 .
00CCH2CH3 . 请写出另外一个同分异构体的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,现有①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3 , 对这四种气体的关系有以下四种表述:
a.体积:②>③>①>④
b.物质的量:②>③>④>①
c.质量:②>③>①>④
d.氢原子个数:①>③>④>②
其中正确的是( )
A.abc
B.bcd
C.abcd
D.acd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种不同质量比的氧化铜与炭粉的混合物样品①、②、③.甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量.
(1)甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热,产生1.12L气体(标准状况),则样品①中氧化铜的质量为g.
(2)乙取样品②ag强热,生成的气体不能使澄清的石灰水变浑浊.再将反应后的固体与足量的稀硝酸微热,充分反应后,有bg固体剩余,该剩余固体的化学式为 . 样品②中氧化铜质量为g (以含a、b的代数式表示).
(3)丙称量样品③强热后剩余的固体,质量比原样品减小了cg,若该固体为金属铜,则样品③中氧化铜物质的量(n)的取值范围为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com