
【题目】根据氢气分子的形成过程示意图(如下图)回答问题:
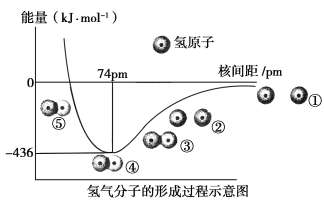
(1)H—H键的键长为________,①~⑤中,体系能量由高到低的顺序是________。
(2)下列说法中正确的是( )
A.氢气分子中含有一个π键
B.由①到④,电子在核间出现的几率增大
C.由④到⑤,必须消耗外界的能量
D.氢气分子中含有一个极性共价键
(3)几种常见化学键的键能如下表:
化学键 | Si—O | H—O | O==O | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 464 | 498 | 176 | x |
请回答下列问题:
①比较Si—Si键与Si—C键的键能大小:x________(填“>”、“<”或“=”)176。
②H2被称为21世纪人类最理想的燃料,而还有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。试计算:每千克H2燃烧(生成水蒸气)放出的热量约为________;每摩尔硅完全燃烧放出的热量约为________。
【答案】(1)74 pm ①⑤②③④ (2)BC
(3)①> ②121500 kJ 990 kJ
【解析】(1)可以直接从题图上有关数据得出,H—H键的键长为74 pm;体系能量由高到低的顺序是①⑤②③④。(2)氢气分子中含有1个σ键,A错;共价键的本质就是高概率地出现在原子间的电子与原子间的电性作用,B正确;④已经达到稳定状态,C正确;氢气分子中含有一个非极性键,D错。(3)①Si—Si键的键长比Si—C键的键长长、键能小。②由题图可知H—H键的键能为436 kJ·mol-1,每千克H2燃烧(生成水蒸气)放出的热量约为1 000 g ÷ 2 g·mol-1 × (464 kJ·mol-1×2-436 kJ·mol-1-498 kJ·mol-1×![]() )=121 500 kJ;每摩尔硅完全燃烧放出的热量约为460 kJ·mol-1×4 mol-498 kJ·mol-1×1 mol-176 kJ·mol-1×2 mol=990 kJ。
)=121 500 kJ;每摩尔硅完全燃烧放出的热量约为460 kJ·mol-1×4 mol-498 kJ·mol-1×1 mol-176 kJ·mol-1×2 mol=990 kJ。


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯。
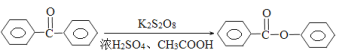
制备苯甲酸苯酯的实验步骤为:
步骤1:将20mL浓H2SO4与40mL冰醋酸在下图装置的烧杯中控制在5℃以下混合。

步骤2:向烧杯中继续加入过硫酸钾25g,用电磁搅拌器搅拌4~5分钟,将二苯甲酮9.1g溶于三氯甲烷后,加到上述混合液中,控制温度不超过15℃,此时液体呈黄色。
步骤3:向黄色液体中加水,直至液体黄色消失,但加水量一般不超过1mL,室温搅拌5h。
步骤4:将反应后的混合液倒入冰水中,析出苯甲酸苯酯,抽滤产品,用无水乙醇洗涤,干燥
(1)步骤1中控制在5℃以下混合的原因为 。
(2)步骤2中为控制温度不超过15℃,向混合液中加入二苯甲酮的三氯甲烷溶液的方法是 。
(3)步骤3中加水不超过1mL,原因是 。
(4)步骤4中抽滤用到的漏斗名称为 。
(5)整个制备过程中液体混合物会出现褐色固体,原因是 ;除去该固体操作为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨分子中的一个氢原子被甲基取代后,所得甲胺(CH3NH2)的性质与氨相似,CH3NH2·H2O也是一元弱碱,25℃时电离常Kb=4.0×10-5。现用0.0500mol/L的稀硫酸滴定10mL 0.1000mol/L的甲胺溶液,溶液中c(OH-)的负对数(pOH)与所加稀硫酸的体积(V)的关系如图所示。下列说法正确的是
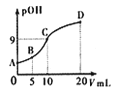
A. 甲胺在水中的电离方程式为:CH3NH2·H2O=CH3NH3++OH-
B. A、B、C三点溶液中,水电离出来的c(H+):B>C>A
C. C点所在溶液中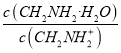 =2.5×10-5
=2.5×10-5
D. B点溶液中存在c(CH3NH2·H2O)>c(CH3NH3+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列改变可确认化学平衡一定移动的是( )
A. 化学平衡常数发生了改变
B. 有气态物质参加的可逆反应达到平衡后,改变了压强
C. 正逆反应速率发生了改变
D. 有固态物质参加的可逆反应达到平衡后,移走适量的固态物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A.纯碱(Na2CO3)从物质的分类看不属于碱
B.由一种元素组成的物质一定是单质
C.凡是能电离出H+的化合物均属于酸
D.盐类物质一定含有金属离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d是四种短周期元素,a、b、d同周期,c、d同主族。a的原子结构示意图为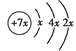 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为![]() 。下列比较中正确的是
。下列比较中正确的是
A. 原子半径:a>c>d>b B. 电负性:a>b>d>c
C. 原子序数:a>d>b>c D. 最高价含氧酸的酸性:c>d>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10 mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA溶液pH的变化曲线如图所示。下列说法正确的是

A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)= c(A-)+c(HA)
D.b点所示溶液中c(A-)> c(HA)
答
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将不同浓度的二元弱酸H2A和NaOH溶液等体积混合(体积变化忽略不计),设计反应后溶液的pH如下表:
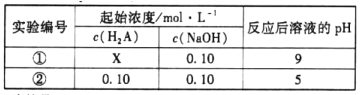
下列判断不正确的是
A.X<0.1
B.HA-的电离程度大于水解程度
C.将实验①所得溶液加水稀释后,c(A2-)/c(HA-)变大
D.实验②所得溶液:c(Na+)=c(A2-)+c(HA-)+c(H2A)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com