
【题目】室温下向10 mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA溶液pH的变化曲线如图所示。下列说法正确的是

A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)= c(A-)+c(HA)
D.b点所示溶液中c(A-)> c(HA)
答
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
物质 | 试剂 | 分离方法 | |
① | 乙烷(乙烯) | H2 | 催化剂加热 |
② | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 过滤 |
③ | 乙醇(水) | 生石灰 | 蒸馏 |
④ | 苯(苯酚) | 浓溴水 | 分液 |
A. ①② B. ①③ C. ③④ D. 只有③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据氢气分子的形成过程示意图(如下图)回答问题:
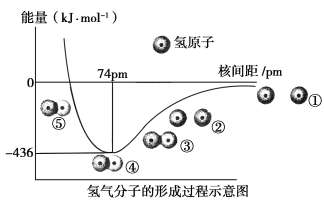
(1)H—H键的键长为________,①~⑤中,体系能量由高到低的顺序是________。
(2)下列说法中正确的是( )
A.氢气分子中含有一个π键
B.由①到④,电子在核间出现的几率增大
C.由④到⑤,必须消耗外界的能量
D.氢气分子中含有一个极性共价键
(3)几种常见化学键的键能如下表:
化学键 | Si—O | H—O | O==O | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 464 | 498 | 176 | x |
请回答下列问题:
①比较Si—Si键与Si—C键的键能大小:x________(填“>”、“<”或“=”)176。
②H2被称为21世纪人类最理想的燃料,而还有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。试计算:每千克H2燃烧(生成水蒸气)放出的热量约为________;每摩尔硅完全燃烧放出的热量约为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述能说明X的非金属性比Y强的是( )
A. Y的单质能将X从NaX的溶液中置换出来
B. Y在暗处可与H2反应,X在加热条件下才能与H2反应
C. X 的气态氢化物比Y的气态氢化物稳定
D. X原子的电子层数比Y原子的电子层数多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH![]() CH3CH3COO﹣+H+ △H>0 ,下列方法中,可以使0.10mol·L﹣1CH3COOH溶液中CH3COOH电离程度增大的是 。
CH3CH3COO﹣+H+ △H>0 ,下列方法中,可以使0.10mol·L﹣1CH3COOH溶液中CH3COOH电离程度增大的是 。
a.加入少量0.10mol·L﹣1的稀盐酸
b.加热
c.加水稀释至0.010mol·L﹣1
d.加入少量冰醋酸
e.加入少量氯化钠固体
f.加入少量0.10mol·L﹣1的NaOH溶液
(2)等物质的量浓度的下列物质的溶液:①NaCl②CH3COONa ③NH4Cl ④AlCl3 ⑤Ba(OH)2 ⑥Na2CO3⑦NaHCO3⑧NaHSO4⑨NaOH ⑩H2SO4其pH值由大到小的顺序是(填序号) 。
(3)限用下列试剂:酚酞、石蕊、稀醋酸、CH3COONa晶体、浓盐酸、Ca(OH)2粉末、CH3COONH4晶体和蒸馏水。根据:①弱酸在水中存在电离平衡;②弱酸根阴离子会破坏水的电离平衡。这两个平衡的移动均会引起指示剂颜色的变化。由此可分别选用上述试剂,设计两种实验证明CH3COOH是弱酸,请简述实验方法及现象。
①应用根据①的实验方法及现象 。
②应用根据②的实验方法及现象 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质的量相等的A、B混合加入2 L的密闭容器中,发生如下反应:3A(气)+B(气) ![]() xC(气)+2D(气)。经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol·(L·min)-1。回答下列问题:
xC(气)+2D(气)。经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol·(L·min)-1。回答下列问题:
(1)x值是____________。
(2)用B表示5 min内的平均反应速率为__________。
(3)反应开始前加入容器中的A、B的物质的量分别为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。

下列说法正确的是( )
A. W、X、Y三种元素氢化物的稳定性依次降低
B. X、Z、W的最高价氧化物对应的水化物酸性最强的是X
C. 五种元素均为非金属元素
D. T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 ( 1 )观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为

① ____________________________________。
② ____________________________________。
( 2 )如图是甲烷燃料电池原理示意图,回答下列问题:

① 电池的负极是________(填“a”或“b”)电极,该极的电极反应式为_____________________。
② 电池工作一段时间后电解质溶液的pH________。(填“增大”“减小”或“不变”)
(3)如图甲乙所示为某实验小组设计的原电池:

①该小组依据的氧化还原反应为(写离子方程式)________ 。
②已知反应前电极质量相等,一段时间后,两电极质量相差12 g,则导线中通过________mol电子。
③用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,发生的离子反应为__________,然后滴加几滴硫氰化钾溶液,溶液变红。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com