
【题目】下列叙述正确的是( )
A.为提醒人们在使用浓H2SO4时要注意安全,贮存浓H2SO4的容器上贴有下图标识
B.实验室可通过蒸馏的方法除去自来水中含有的Cl-等杂质制蒸馏水
C.做焰色反应实验时,应先将铂丝(或铁丝)用稀硫酸洗净后,在酒精灯外焰上灼烧至没有颜色时,再蘸取待检溶液进行实验
D.由于碱金属单质化学性质活泼,实验室中的各种碱金属单质均保存在煤油中
【答案】B
【解析】解:A.浓硫酸具有强的腐蚀性,属于腐蚀性的药品,不是剧毒品,A不符合题意;
B.在自来水中含有多种可溶性的盐,由于水的沸点只有100度,而盐的沸点高,所以可以用蒸馏的方法使水变为气态,从而可除去自来水中含有的Cl-等杂质制蒸馏水,B符合题意;
C.做焰色反应实验时,应先将铂丝(或铁丝)用稀硫酸洗净后,在酒精灯外焰上灼烧至与酒精灯火焰的颜色相近时,再蘸取待检溶液进行实验,C不符合题意
D.由于碱金属单质化学性质活泼,实验室中的各种碱金属单质要密封保存,Li的密度比煤油小,不能保存在煤油中,D不符合题意。
所以答案是:B
【考点精析】解答此题的关键在于理解碱金属的性质的相关知识,掌握原子半径为同周期最大,易失电子.强还原剂且从Li→Cs金属性增强;取高价氧化物的水化物呈强碱性,从Li→Cs碱性增强,以及对蒸馏与分馏的理解,了解蒸馏是将液态物质加热到沸腾变为蒸气,又将蒸气冷却为液体这两个过程联合操作.用这一操作可分离、除杂、提纯物质;分馏和蒸馏一样,也是利用混合物中各物质的沸点不同,严格控制温度,进行分离或提纯物质的操作,是多次的蒸馏.


科目:高中化学 来源: 题型:
【题目】某同学设计如下元素周期表,以下说法正确的是( )
A.X、Y、Z元素分别为N、P、O
B.白格中都是主族元素,灰格中都是副族元素
C.原子半径:Z>X>Y
D.X、Y、Z的气态氢化物中最稳定的是Y的氢化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下在一容积恒为2L的容器内发生反应:2A(g)+B(g) ![]() 2C(g),已知起始投入4mol A(g)和2mol B(g),经2s后测得C的浓度为0.6mol/L,并且2s后各组分浓度不再改变.下列说法正确的是( )
2C(g),已知起始投入4mol A(g)和2mol B(g),经2s后测得C的浓度为0.6mol/L,并且2s后各组分浓度不再改变.下列说法正确的是( )
A.2s内用物质A表示的平均反应速率为0.6mol/(Ls)
B.2s内用物质B表示的平均反应速率为0.6mol/(Ls)
C.2s后每有0.6mol的物质B生成,同时就有0.6mol物质C生成
D.2s时物质B的浓度为0.7mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.23 g金属钠投入到100 ml水中,使其充分反应,假设反应后溶液的体积不变。试计算:
(1)反应后所得溶液溶质的物质的量浓度是多少?
(2)产生标准状况下的气体多少毫升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下每个选项中的两组物质都能反应,且放出同一种气体产物的是( )
A.铜与稀硫酸,铜与浓硫酸
B.铁与稀硫酸,铁与浓硫酸
C.硫化钠与稀硫酸,亚硫酸钠与稀硫酸
D.硫化钠与稀硫酸,硫化钠与稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2是重要化学物质,某学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其流程如图: 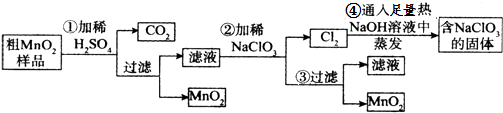
按要求回答下列问题
(1)第②步操作中,氧化性强弱顺序:ClO3﹣MnO2 (填“>”“<”),写出操作②中发生反应的离子方程式;当反应中转移2mol电子时,生成的氧化产物的物质的量为mol.
(2)第④步操作中,最终得到的固体除NaClO3外,还一定含有下列物质中的 .
a.NaCl b.NaClO c.NaClO4 d.NaOH
(3)为得到纯净的MnO2 , 须将过滤后的MnO2合并后进行洗涤,判断是否洗涤干净可选用的试剂是(填写一组即可).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com