
【题目】生物大分子在生物体的生命活动中具有重要作用,构成生物大分子的最基本元素是
A. C B. H C. O D. N
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】氢气是合成氨的重要原料,合成氨反应的热化方程式如下:
N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol
2NH3(g) ΔH=-92.4 kJ/mol
(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。

图中t1时引起平衡移动的条件可能是 ,其中表示平衡混合物中NH3的含量最高的一段时间是 ,若t0-t1,t1-t3,t3-t5这三段平衡常数分别用K1,K2,K3表示,那么K1,K2,K3的大小关系是____________。
(2)若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“ 向右”或“不”);使用催化剂反应的ΔH (填“增大”、“减小”或“不改变”)。
(3)温度为T ℃时,将2a mol H2和 a mol N2放入0.5 L密闭容器中,充分反应后测得N2的转化率为50%。则反应的平衡常数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关HCl和HBr的叙述错误的是
A. 键能:HBr>HCl B. 键长:HBr>HCl
C. 沸点:HBr>HCl D. 共用电子对偏向:HCl>HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中能大量共存,加入OH-有沉淀产生,加入H+有气体放出的是
A.Na+、Cu2+、Cl-、SO![]() B.Fe3+、K+、SO
B.Fe3+、K+、SO![]() 、NO
、NO![]()
C.Na+、CO![]() 、OH-、NO
、OH-、NO![]() D.Na+、Ca2+、Cl-、HCO
D.Na+、Ca2+、Cl-、HCO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】模拟铁的电化学防护的实验装置如图所示,下列说法不正确的是
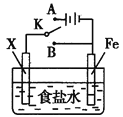
A.若X为碳棒,开关K置于A处可减缓铁的腐蚀
B.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀
C.若X为锌棒,开关K置于B处时,铁电极上发生的反应为2H++2e-=H2↑
D.若X为碳棒,开关K置于A处时,铁电极上发生的反应为2H++2e-=H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )

A. 升高温度,可能引起由c向b的变化
B. 该温度下,水的离子积常数为l.0×10-13
C. 该温度下,加入FeCl3可能引起由b向a的变化
D. 该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域中有重要用途。
Ⅰ.工业上有多种方法来制备氮化硅,下面是几种常见的方法:
(1)方法一 直接氮化法:在1300~1400 ℃时,高纯粉状硅与纯氮气化合,其反应方程式为3Si+2N2![]() Si3N4
Si3N4
(2)方法二 可以用NH3和SiH4(硅烷)在一定条件下反应,并在600 T的加热基板上生成氮化硅膜,其反应方程式为___________________。
(3)方法三 化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和HCl,与方法一相比,用此法制得的氮化硅纯度较高,其原因是___________________。
(4)方法四 Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体__________________(填分子式);然后使Si(NH2)4受热分解,分解后的另一种产物的分子式为_________________。
Ⅱ.工业上制取高纯硅和四氯化硅的生产流程如下:
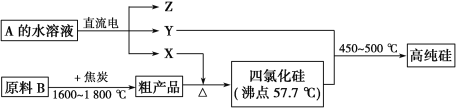
已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(1)写出焦炭与原料B中的主要成分反应的化学方程式:__________________
(2)上述生产流程中电解A的水溶液时,以Cu为阳极电解A的水溶液电解反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
下列叙述不正确的是
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.放电时阳极反应为: Fe(OH)3+5OH--3e-= FeO42-+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时的正极在充电时应接电源正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com