
| A. | 硝酸与铜反应得到NO2、N2O4共23g,则铜失去的电子数为0.5NA | |
| B. | 3g甲酸与乙醛的混合物中含有共价键为0.4NA | |
| C. | 将标准状况下2.24LSO2通入水中完全溶解,溶液H2SO3分子数为0.1NA | |
| D. | 标准状况下8.96L的平均相对分子质量为3.5的H2与D2含有中子数0.3NA |
分析 A、NO2、N2O4的最简式均为NO2,且每当生成1molNO2,硝酸得1mol电子;
B、甲酸和乙醛的摩尔质量不同;
C、二氧化硫和水的反应为可逆反应;
D、H2与D2的相对分子质量分别为2和4,根据十字交叉法求出两者的比例.
解答 解:A、NO2、N2O4的最简式均为NO2,故23g混合物中含有的NO2的物质的量为0.5mol,且每当生成1molNO2,硝酸得1mol电子,故当生成0.5molNO2时反应转移0.5mol电子,即同失去0.5NA个电子,故A正确;
B、甲酸和乙醛的摩尔质量不同,且无相同的最简式,故混合物中的共价键条数无法计算,故B错误;
C、二氧化硫和水的反应为可逆反应,不能进行彻底,且生成的亚硫酸分子能部分电离,故溶液中的亚硫酸分子个数小于0.1NA个,故C错误;
D、H2与D2的相对分子质量分别为2和4,根据十字交叉法可知H2与D2的物质的量之比为1:3,故8.96L即0.4mol的混合气体中H2的物质的量为0.1mol,而D2的物质的量为0.3mol,而H2中不含中子,D2中含2个中子,故0.3molD2中含0.6mol中子即0.6NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意公式的运用和物质的结构特点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Al3+、HCO3-、NO3- | B. | AlO2-、Cl-、Mg2+、K+ | ||
| C. | NH4+、Na+、CH3COO-、NO3- | D. | Na+、NO3-、ClO-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | C-C | C═C | C≡C | C-H | H-H | Cl-Cl | H-Cl |
| 键焓(△H)/kJ•mol-1 | 347.7 | 615.0 | 812.0 | 413.4 | 436.0 | 242.7 | 431 |
| A. | CH2═CH2(g)+H2(g)→CH3CH3(g)△H=+123.5 kJ•mol-1 | |
| B. | CH≡CH(g)+2H2(g)→CH3CH3(g)△H=-317.3 kJ•mol-1 | |
| C. | 稳定性:H-H键<H-Cl键<C-H键 | |
| D. | 由上表数据可计算乙烷与氯气发生一氯代反应的焓变(△H) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13.6g | B. | 12g | C. | 6g | D. | 3.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 己烷(己烯) | 溴水 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | 苯(苯酚) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | KMnO4酸性溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
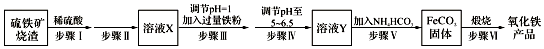
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2溶液与K3[Fe(CN)6]混合后得到特征蓝色沉淀,利用此反应可检验Fe2+ | |
| B. | 向饱和食盐水中加入少量浓盐酸,看到溶液振荡,溶液变浑浊 | |
| C. | 某温度下,向AgCl饱和溶液中加入蒸馏水,AgCl的溶解度、Ksp均增大 | |
| D. | 处理含有Hg2+离子的废水可加入硫化钠,使Hg2+离子转化为HgS沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com