
���� ��1����ͭ�Ĵ������£������ͷ�����Ӧ����A��B��AΪ��Σ�Ϊ����泥�B�ڱ�״����Ϊ��̬���ڴ˷�Ӧ�У���ÿ��Ӧ1���������ͬʱ��Ӧ0.75��������������ͷ����ļ�����֮����1��0.75=4��3����ÿ��Ӧ8.96L��������״������ͬʱ����0.3molA�������ͷ���淋ļ�����֮��=$\frac{8.96L}{22.4L/mol}$��0.3mol=4��3������ԭ���غ�֪�����ɵ���һ��������NF3�������ͷ�����Ӧ���ɷ���狀�������������Ӧ����ʽΪ��4NH3+3F2 $\frac{\underline{\;Cu\;}}{\;}$NF3+3NH4F���ݴ˼������ת�ƣ�
��2���������ʵ���Fe2O3��FeCl3�����ܱչ��м��ȣ���ǡ����ȫ��Ӧ����ֻ����һ�ֲ���X�������ʵ����Ƿ�Ӧ�������ʵ�����1.5�������ݷ�Ӧǰ��ԭ���غ�����ж�X�Ļ�ѧʽ��
��3�����������������Ԫ�ػ��ϼ�+7�۱仯Ϊ+2�ۣ����������������Ԫ��+4�۱仯Ϊ+6�ۣ�����ת������10����ϵ����غ��ԭ���غ���ƽ��д���ӷ���ʽ��
��� �⣺��1���������л�ԭ�ԣ���ͭ�Ĵ������£������ͷ���������Ӧ����A��B��AΪ��Σ�B�ڱ�״����Ϊ��̬���ڴ˷�Ӧ�У�����1��������μӷ�Ӧ������0.75��������μӷ�Ӧ�������ͷ����ļ�����֮����1��0.75=4��3������8.96L��������״�����μӷ�Ӧ��������0.3mol A�������ͷ���淋ļ�����֮��=$\frac{8.96L}{22.4L/mol}$��0.3mol=4��3����Ӧ����ʽΪ��4NH3+3F2 $\frac{\underline{\;Cu\;}}{\;}$NF3+3NH4F����Ӧ�е���ת��6e-������3mol�ڱ�״���£�����2.24L BΪNF3Ϊ0.1mol����÷�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ0.6mol��
�ʴ�Ϊ��0.6��
��2���������ʵ���Fe2O3��FeCl3�����ܱչ��м��ȣ���ǡ����ȫ��Ӧ����ֻ����һ�ֲ���X�������ʵ����Ƿ�Ӧ�������ʵ�����1.5������Fe2O3��FeCl3���ʵ�������1mol������X���ʵ���Ϊ3mol��Fe2O3+FeCl3=3X��������ԭ���غ�õ���XΪFeOCl��
�ʴ�Ϊ��FeOCl��
��3�����������������Ԫ�ػ��ϼ�+7�۱仯Ϊ+2�ۣ����������������Ԫ��+4�۱仯Ϊ+6�ۣ�����ת������10������д�õ����ӷ���ʽΪ��
2MnO4-+5SO32-+6H+=2Mn2++5SO42-+3H2O��
�ʴ�Ϊ��2�� 5�� 6H+��2�� 5�� 3H2O��
���� ���⿼���������ƶϡ�������ԭ����ʽ����ƽ������ԭ���غ�ķ���Ӧ�ã�ע�������������Ϣ������Ӧ�ã����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�


 �п������п��Ծ����ϵ�д�
�п������п��Ծ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ | Fe��OH��3 | Al��OH��3 | Fe ��OH��2 | Cu ��OH��2 |
| pH | 3.4 | 5.2 | 9.7 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������CO2��ˮ�����Ļ��������������Na2O2��ַ�Ӧ�����ձ�����NaOH | |
| B�� | ������MnO2�뺬4molHCl��Ũ������ȳ�ַ�Ӧ��������Cl2��Ϊ1mol | |
| C�� | ��2molHCl��ij�������������̼������Һ�г�ַ�Ӧ�õ�CO2�����Ϊ1mol | |
| D�� | �����Ķ�����̼ͨ��ƫ��������Һ�У��������ɵIJ����ΪAl��OH��2��̼������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ij��ѧС�������ͭ��Ũ��ϡ���ᷴӦ��һ�廯ʵ��װ����ͼ��ʾ�����̶ֹ�װ��ʡ�ԣ���ʵ�鲽�����£���ش��������⣺
ij��ѧС�������ͭ��Ũ��ϡ���ᷴӦ��һ�廯ʵ��װ����ͼ��ʾ�����̶ֹ�װ��ʡ�ԣ���ʵ�鲽�����£���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ������������MnO2+2Cl-+4H+$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O | |
| B�� | ʵ�����ƶ�������Cu+SO42-+4H+$\frac{\underline{\;\;��\;\;}}{\;}$Cu2++SO2��+2H2O | |
| C�� | ʵ������Ũ��ˮ����ʯ���ư�����NH3•H2O+CaO�TCa��OH��2+NH3�� | |
| D�� | ʵ�����ƶ���������3Cu+4H++2NO3-�T3Cu2++2NO2��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
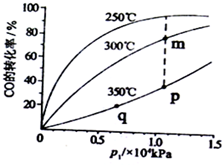 ͨ����ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ�ϣ���ҵ����CO��H2�ϳ�CH3OH����ش��������⣮
ͨ����ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ�ϣ���ҵ����CO��H2�ϳ�CH3OH����ش��������⣮| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | ||
| H2O | CO��g�� | H2 | CO��g�� | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 1.5 | 2 |
| 3 | 2 | 4 | 1.0 | n | t | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͭ��Ӧ�õ�NO2��N2O4��23g����ͭʧȥ�ĵ�����Ϊ0.5NA | |
| B�� | 3g��������ȩ�Ļ�����к��й��ۼ�Ϊ0.4NA | |
| C�� | ����״����2.24LSO2ͨ��ˮ����ȫ�ܽ⣬��ҺH2SO3������Ϊ0.1NA | |
| D�� | ��״����8.96L��ƽ����Է�������Ϊ3.5��H2��D2����������0.3NA |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com