
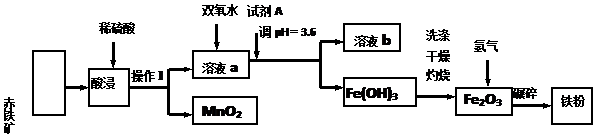
| ������ | Fe��OH��3 | Al��OH��3 | Fe ��OH��2 | Cu ��OH��2 |
| pH | 3.4 | 5.2 | 9.7 | 6.7 |
���� ��������Ҫ�ɷ�Ϊ60.0%Fe2O3��������3.6%FeO��Al2O3��MnO2��CuO�ȣ��������ܽ⣬����������ת��Ϊ���������ӣ��������費�ܣ��ټ�˫��ˮ���������ӻ�ԭΪ�����ӣ�����PH=3.6���������������������ˣ�����������������������������������ԭ�������ʣ��Դ˽����⣮
��� �⣺��������Ҫ�ɷ�Ϊ60.0%Fe2O3��������3.6%FeO��Al2O3��MnO2��CuO�ȣ��������ܽ⣬����������ת��Ϊ���������ӣ��������費�ܣ��ټ�˫��ˮ���������ӻ�ԭΪ�����ӣ�����PH=3.6���������������������ˣ�����������������������������������ԭ�������ʣ�
��1�������ʵij�����ʹ��ǰҪ������飬���������Һ�Ӵ�������ӿ������Ӧ���ʣ���߽����ʣ�ͨ���������ܵĶ������̹��˵���
�ʴ�Ϊ�������Һ�Ӵ�������ӿ������Ӧ���ʣ���߽����ʣ����ˣ�
��2��MnO2��KClO3��KOH��Һ��Ϲ��ȣ��ɵõ�K2MnO4����Ԫ�ػ��ϼ����ߣ�����Ԫ�ػ��ϼ۽��ͣ��������Ȼ��أ���ѧ����ʽΪ��3MnO2+KClO3+6KOH$\frac{\underline{\;\;��\;\;}}{\;}$3K2MnO4+KCl+3H2O��
�ʴ�Ϊ��3MnO2+KClO3+6KOH$\frac{\underline{\;\;��\;\;}}{\;}$3K2MnO4+KCl+3H2O��
��3�����ݱ������ݿ�֪��Ϊ��֤������ȫ��������PH����3.4����Ϊ�˲�ʹ�����������ӳ�����PH����̫��Ksp[Cu��OH��2]=c��Cu2+����c2��OH-��=2��10-20��c��H+��=$\frac{Kw}{c��O{H}^{-}��}$����ӦCu2++2H2O?Cu��OH��2+2H+��ƽ�ⳣ��K=$\frac{{c}^{2}��{H}^{+}��}{c��C{u}^{2+}��}$=$\frac{Kw}{c{{\;}^{2}��}^{\;}O{H}^{-}��c��C{u}^{2+}��}$=$\frac{Kw}{Ksp[Cu��OH��_{2}]}$=5��10-9��
�ʴ�Ϊ��ʹ������ȫ�����������������������Ӳ�������5��10-9��
��4��˫��ˮ�����������ӣ�H2O2+2Fe2++2H+=2Fe3++2H2O��
�ʴ�Ϊ��H2O2+2Fe2++2H+=2Fe3++2H2O��
��5��������ʯ1kg���������ʵ���Ϊ��$\frac{1000��60%}{160}��2$+$\frac{1000��3.6%}{72}$=8mol�����������ʵ���Ϊ��$\frac{17g}{17g/mol}$=1mol�����Ͱ��������ʵ���֮����8��1�����ɵĵ�����ΪFe8N�����������غ㣬��÷�ӦΪ��16Fe+2NH3$\frac{\underline{\;����500��\;}}{\;}$2Fe8N+3H2��
�ʴ�Ϊ��16Fe+2NH3$\frac{\underline{\;����500��\;}}{\;}$2Fe8N+3H2��
���� ���⿼�鹤ҵ���̣��漰���ܵ���ʵ��ܽ�ƽ��ͳ���ת����Ϊ�߿��������ͣ�ע��������ԭ��Ӧ���������ݵ�Ӧ�ã���Ŀ�Ѷ��еȣ�


 ��Կ���Ծ�ϵ�д�
��Կ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCO3- | B�� | SO${\;}_{4}^{2-}$ | C�� | NH${\;}_{4}^{+}$ | D�� | Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �٢� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 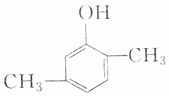 �� ��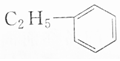 | B�� |  �� ��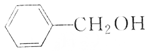 | ||
| C�� | 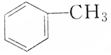 �� �� | D�� | CH3CH2OH��CH2OH-CH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 463kJ•mol-1 | B�� | 926kJ•mol-1 | C�� | 1852kJ•mol-1 | D�� | 920kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ����Һ��һ������SO42-��NH4+��CO32-��Cl-������ | |
| B�� | ����Һ�����ٺ���0.23g Na+ | |
| C�� | ����Һ�п��ܺ���Mg2+��Cl- | |
| D�� | ����Һ�к���0.355g Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CaO+H2O�TCa��OH��2�����Էų��������ȣ��ʿɰѸ÷�Ӧ��Ƴ�ԭ��أ������еĻ�ѧ��ת��Ϊ���� | |
| B�� | ������������ͬ�����С����š���ԭ��رȲ��������š���ԭ��ص�������ʱ�䳤 | |
| C�� | ԭ��ع���ʱ����������һ�������ݲ��� | |
| D�� | ����ˮբ����������������ӵ�����������������ֹ�丯ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com