
在无色透明酸性溶液中,能大量共存的离子组是
A.Mg2+、NO3-、Cl、Na+ B.K+、SO42-、HCO3-、Na+
C.NH4+、NO3-、Al3+、CH3COO D.MnO4-、K+、SO42-、Na+
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列类比分析结果正确的是
A.Fe3O4根据化合价规律可表示为FeO·Fe2O3,则Pb3O4也可表示为PbO·Pb2O3
B.CaC2能水【解析】
CaC2 + 2H2O = Ca(OH)2 + C2H2 ↑,则Al4C3也能水【解析】
A l4C3 + 12H2O = 4A1(OH)3↓+ 3CH4↑
l4C3 + 12H2O = 4A1(OH)3↓+ 3CH4↑
C.Cl2与Fe加热生成FeCl3,则I2与Fe加热生成Fe I3
D.SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液也不产生沉淀
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北大附中河南分校高二上9月考化学试卷(解析版) 题型:选择题
下列变化中,属于放热反应的是
A.H2O(g)═H2O(l)△H=﹣44kJ/mol
B.2HI(g)═H2(g)+I2(g)△H=+14.9kJ/mol
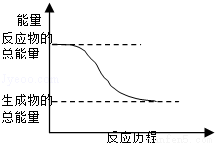
C.能量变化如图所示的化学反应
D.形成化学键时放出能量的化学反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北京大学附属中学分校高二上抽考化学试卷(解析版) 题型:填空题
(12分)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ΔH1 <0(I)
NaNO3(s)+ClNO(g) K1 ΔH1 <0(I)
2NO(g)+Cl2(g) 2ClNO(g) K2 ΔH2 <0(II)
2ClNO(g) K2 ΔH2 <0(II)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
(用K1、K2表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应(II)达到平衡。
测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后n(Cl2)= mol,NO的转化率α1= 。其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率α2 α1(填“>”“<”或“=”),平衡常数K2 (填“增大”“减小”或“不变”)。若要使K2减小,可采用的措施是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北京大学附属中学分校高二上抽考化学试卷(解析版) 题型:选择题
对可逆反应2A(s)+3B(g)  C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①② B.④ C.③ D.④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一上期中测试化学试卷(解析版) 题型:选择题
下列两种物质的溶液混合后,能发生离子反应,且溶液的总质量不会发生改变的是
A.石灰水和稀盐酸混合
B.小苏打溶液和柠檬水混合
C.人工盐(含有硫酸钠、碳酸氢钠、氯化钠、硫酸钾)溶液与BaCl2溶液混合
D.氯化钠溶液和蔗糖水混合
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁师大附属中学高二10月月考化学试卷(解析版) 题型:选择题
可逆反应N2(g)+3H2(g) 2NH3(g),△H=-Q KJ/mol(Q>0)。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molN2和3molH2,在一定条件下达到平衡时放出热量为Q1KJ;在相同条件下,向乙容器中加入2molNH3达到平衡后吸收热量为Q2KJ,已知Q1=4Q2。下列叙述不正确的是
2NH3(g),△H=-Q KJ/mol(Q>0)。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molN2和3molH2,在一定条件下达到平衡时放出热量为Q1KJ;在相同条件下,向乙容器中加入2molNH3达到平衡后吸收热量为Q2KJ,已知Q1=4Q2。下列叙述不正确的是
A.达到平衡时,两容器中反应物的转化率不同
B.达到平衡时,甲中NH3的体积分数与乙相等
C.达到平衡后,再向乙中加入0.2moLN2、0.6molH2、1.6molNH3,平衡向生成NH3的方向移动
D.乙中的热化学反应方程式为2NH3(g) N2(g)+3H2(g);△H=+Q2KJ/mol
N2(g)+3H2(g);△H=+Q2KJ/mol
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期四调考试化学试卷(解析版) 题型:选择题
已知离子方程式:As2S3+H2O+NO3-→AsO43—+SO42—+NO↑+H+(未配平),下列说法错误的是
A.配平后水的化学计量数为4
B.反应后溶液呈酸性
C.配平后氧化剂与还原剂的物质的量之比为3∶28
D.氧化产物为AsO43—和SO42—
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一上10月月考化学试卷(解析版) 题型:填空题
(10分)现用18.4 mol·L-1的浓硫酸来配制450mL 0.2 mol·L-1的稀硫酸,可供选择的仪器有:
①玻璃棒 ②烧杯 ③胶头滴管 ④量筒 ⑤托盘天平
(1)上述仪器在配制过程中不需要用到的是__________________(填序号)除上述仪器外,尚缺最重要的仪器是
(2)计算所需浓硫酸的体积为___________mL。(精确到一位小数)
(3)实验中用到玻璃棒,其作用分别是:___________、__________。
(4)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却。
其正确的操作顺序为:②→①→③→_________→_________→_________→_________→④(填序号)
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有____________(填序号)
①定容时,仰视刻度线。
②未冷却至室温就转移到容量瓶中。
③容量瓶中含有少量蒸馏水。
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒。
⑤定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com