
【题目】某碱金属M及其氧化物(M2O)组成的混和物13.3g,加足量水充分反应后的溶液经蒸发结晶,得干燥固体16.8g,求该混和物的成分_________及其质量____________。
【答案】K,K2O 9.4g,3.9g
【解析】
解答本题关键是取极值法:假设13.3g全部是碱金属M,根据生成碱的质量,通过方程式列出比例式,计算M的相对原子质量,再假设13.3g全部是氧化物M2O根据生成碱的质量,通过方程式列出比例式,计算M的相对原子质量,进而判断元素名称。
根据碱金属和水反应的通式进行计算。由2M+2H2O=2MOH+H2![]() ,M2O+H2O=2MOH反应可知,设金属M的相对原子质量为a,假设13.3g全部是碱金属,则
,M2O+H2O=2MOH反应可知,设金属M的相对原子质量为a,假设13.3g全部是碱金属,则![]() =
=![]() ,解得约a=65;假设13.3g全部是氧化物(M2O),则
,解得约a=65;假设13.3g全部是氧化物(M2O),则![]() =
=![]() ,解得约a=25;根据碱金属相对原子质量为25<a<65,所以M为钾;设钾的质量为xg,氧化钾的质量为yg,则有x+y= 13.3;(
,解得约a=25;根据碱金属相对原子质量为25<a<65,所以M为钾;设钾的质量为xg,氧化钾的质量为yg,则有x+y= 13.3;(![]() +
+![]() )
)![]() (39+17)= 16.8;解得x=9.4g;y=3.9g;答案:K,K2O;9.4g,3.9g。
(39+17)= 16.8;解得x=9.4g;y=3.9g;答案:K,K2O;9.4g,3.9g。


科目:高中化学 来源: 题型:
【题目】某小组在Fe2+检验实验中观察到异常现象,为探究“红色褪去”的原因,进行如下实验:
编号 | 实验I | 实验II | 实验III |
实验步骤 |
| 将实验I褪色后的溶液分三份分别进行实验
| 为进一步探究“红色褪去”的原因,又进行以下实验 ① ②取反应后的溶液,滴加盐酸和BaCl2溶液 |
现象 | 溶液先变红,片刻后红色褪去,有气体生成(经检验为O2) | ①无明显现象 ②溶液变红 ③产生白色沉淀 | ①溶液变红,一段时间后不褪色。 ②无白色沉淀产生 |
分析上述三个实验,下列叙述不正确的是
A.在此实验条件下H2O2氧化Fe2+的速率比氧化SCN-的速率快
B.通过实验Ⅱ推出实验Ⅰ中红色褪去的原因是由于SCN-被氧化
C.通过实验Ⅰ和实验Ⅲ对比推出红色褪去只与H2O2的氧化性有关
D.综上所述,实验Ⅰ中红色褪去的原因与化学平衡移动原理无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NH3 通入50 mL NH4Cl 溶液中至pH=10,再向其中滴加1 mol/L盐酸。溶液的pH随加入盐酸体积的变化如图所示,下列说法不正确的是

A.a 点溶液中,c(OH-) = 1×10-4mol/LB.b 点溶液中,c(![]() ) > c(Cl-)
) > c(Cl-)
C.a→b,水的电离程度减小D.c 点时,加入的 n(HCl)小于通入的 n(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备。下列说法中正确的是
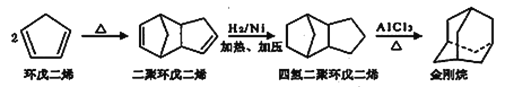
A. 环戊二烯中的所有原子共平面 B. 二聚环戊二烯的分子式为C10H10
C. 四氢二聚环戊二烯与金刚烷互为同系物 D. 金刚烷的一氯一溴代物有8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A经李比希法和质谱法分析得知其分子式为C8H8O2,相对分子质量为136,A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环,且苯环上只有一个取代基,其核磁共振氢谱与红外光谱如图。关于A的下列说法中不正确的是( )
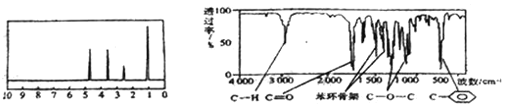
A.A分子属于酯类化合物,在一定条件下能发生水解反应
B.A在一定条件下可与3molH2发生加成反应
C.符合题中A分子结构特征的有机物只有一种
D.与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别进行下表所示实验,实验现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 测量熔融状态下NaHSO4的导电性 | 能导电 | 熔融状态下NaHSO4能电离出Na+、H+、 |
B | 蘸有浓氨水的玻璃棒靠近X | 有白烟产生 | X可能为浓盐酸 |
C | 将甲烷与氯气按体积比1:4混合于试管中光照 | 反应后混合气体能使润湿的石蕊试纸变红 | 生成的氯代甲烷具有酸性 |
D | 将AlCl3溶液加热蒸干 | 得到白色固体 | 白色固体成分为纯净的AlCl3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易反应,生成一种氯化物和两种常见的氮氧化物,其中一种呈红棕色。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:
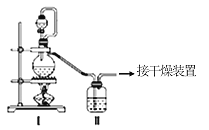
为制备纯净干燥的气体,下表中缺少的药品是:
制备原料 | 装置Ⅰ | 装置Ⅱ | |
烧瓶中 | 分液漏斗中 | ||
制备纯净Cl2 | MnO2 | ①________ | 饱和食盐水 |
制备纯净NO | Cu | 稀硝酸 | ②________ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
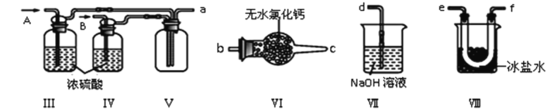
①装置连接顺序为a→_______(按气流自左向右方向,用小写字母表示)。
②为了使实验顺利进行,实验中先通入的气体是_____(填Cl2或NO),待装置Ⅴ中充满气体时,再将另一气体缓缓通入,此操作的目的是_____。
③装置Ⅴ生成NOCl的化学方程式是_____。
④装置Ⅵ的作用为_____,若无该装置,Ⅷ中NOCl可能发生反应的化学方程式为_______。
(3)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用c mol/LAgNO3 标准溶液滴定至终点,消耗标准溶液的体积为b mL。亚硝酰氯(NOCl)的质量分数为_________(用代数式表示即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨既是实验室中常用试剂,也是工业上重要原料。
(1)某学习小组欲制备少量的氨水。供选用的试剂有:①NH4Cl②(NH4)2CO3 。提供的装置如下,请回答下列问题:
①装置A试管内发生反应的化学方程式为__________;
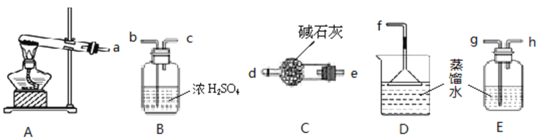
②从提供的仪器中选择并组装一套本实验的合理、简洁装置,按气流方向连接顺序为(用图中标注的导管口符号表示)a→____;
(2)氨在氧气中燃烧,生成水和一种单质。
已知:N2(g)+3H2(g)2NH3(g)△H= -92.4kJ·mol-1
2H2(g)+ O2(g)= 2H2O(l)△H= -572kJ·mol-1
写出氨在氧气中燃烧生成液态水和气态单质的热化学方程式:_________;
(3)已知在一定条件下,将1molN2和3molH2混合于一个10L的密闭容器中发生的反应为N2+3H2![]() 2NH3,5min后达到平衡,平衡时氨的体积分数为25%。
2NH3,5min后达到平衡,平衡时氨的体积分数为25%。
①该反应的平衡常数=_____;
②从反应开始到平衡时,N2的反应速率![]() (N2)=______;
(N2)=______;
(4)工业上以氨气、空气为主要原料制取硝酸。在容积恒定的密闭容器中进行反应2NO(g)+O2(g)2NO2(g)△H>0。该反应的反应速率(![]() )随时间(
)随时间(![]() )变化的关系如图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)______。
)变化的关系如图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)______。

A.在![]() 时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
B.在![]() 时,采取的措施可以是升高温度
时,采取的措施可以是升高温度
C.在![]() 时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
D.在![]() 时,容器内NO2的体积分数是整个过程中的最大值
时,容器内NO2的体积分数是整个过程中的最大值
(5)为检验氨气与酸反应得到的某种常见氮肥的成分,某同学进行了以下实验:①加热氮肥样品产生气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊。②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。由此可知该氮肥的主要成分可能是_____________(填选项序号);
A.NH4Cl B.(NH4)2CO3C.NH4HCO3D.NH4NO3
(6)硝酸厂常用Na2CO3溶液吸收处理尾气NO2生成CO2。若9.2g NO2和Na2CO3溶液完全反应时转移电子0.1mol,则反应的离子方程式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某有机物A的结构,做如下实验:

①将4.4g该有机物完全燃烧,生成 0.2mol CO2和3.6g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③A的核磁共振氢谱如图2:
试回答下列问题:
(1)有机物A的相对分子质量是_____________
(2)有机物A的实验式是_____________
(3)有机物A的分子式是_____________
(4)红外光谱上发现A有﹣COOH和2个﹣CH3则有机物A的结构简式 ________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com