
下列图示所表示的实验设计正确的是
A.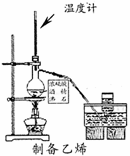 B.
B.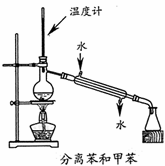
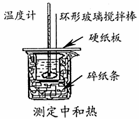 D.
D.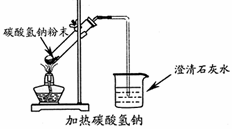
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
N2(g)+3H2(g) ![]() 2NH3(g);ΔH<0
2NH3(g);ΔH<0

请根据图示回答下列问题:
(1)反应起始时,氮气与氢气的物质的量之比n(N2)∶n(H2)= _________∶_________。在15分钟时合成氨反应第一次达到平衡,其间以H2的浓度变化所表示的平均化学反应速率为_________________________。
(2)在t1时,曲线发生变化的原因是__________________、__________________。请计算氢气在t1起点时的坐标(_________,_________)以及在t2平衡时的坐标(_________,_________)。并在图中画出在t1—t2之间氢气的物质的量变化曲线。
(3)为达到图示中t2的平衡状态,在t1—t2之间需要采取的措施是_________。
a.扩大容器的体积
b.升高温度
c.降低温度
d.缩小容器的体积
(4)经历十次上述的循环过程,计算在t11达到平衡时,N2和H2的物质的量之比n(N2)∶n(H2)= _________∶_________,整个过程中N2和H2的总转化率之比α(N2)∶α(H2)= _________∶_________。
(5)根据以上计算结果,请你建议合成氨反应的最佳原料比是:n(N2)∶n(H2)=_________。
查看答案和解析>>
科目:高中化学 来源:2010—2011学年广东省培正中学高一下学期期中考试化学试卷 题型:填空题
(本题有3小题)(共10分)
I.(2分)下列两个图示,A所表示的是--------------热反应,B所表示的是--------------热反应。
A B
II.(2分)在氢气与氯气反应生成氯化氢气体的反应中,若断裂1mol H - H键要吸收436KJ的能量,断裂1mol Cl- Cl键要吸收243KJ的能量,断裂1molH - Cl键要吸收432KJ的能量,则表示1mol 氢气在氯气中充分燃烧的热化学方程式是 。
III.(5分)如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5ml盐酸于试管中,试回答下列问题:
(1)实验中观察到的现象是试管中 ,烧杯中析出晶体。
(2)写出试管中反应的离子反应方程式 ,
(3)由此推知,MgCl2溶液和H2的总能量 填(“大于”“小 于”或“等于”)镁片和盐酸的总能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com