
下列FeCl3的性质中,能够证明FeCl3是共价化合物的是( )
A.FeCl3易溶于水
B.液态的FeCl3不导电
C.FeCl3常温下不易分解
D.FeCl3溶于水能电离,呈酸性
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:2017届宁夏高三上学期统练二化学试卷(解析版) 题型:选择题
某温度下,体积一定的密闭容器中发生如下可逆反应X(g)+mY(s) 3Z(g) △H,下列说法正确的是( )
3Z(g) △H,下列说法正确的是( )
A.气体的平均密度不变时.说明达到了平衡状态
B.加入少量的X,△H变大
C.加入一定量:的惰性气体,平衡向左移动
D.加入少量的Y正反应速率加快
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学试卷(解析版) 题型:填空题
尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
(1)恒温恒容下,在某密闭容器中充入CO(NH2)2和H2O,在120℃、催化剂作用下发生反应:CO(NH2)2 (s) + H2O(g) 2 NH3(g)+CO2(g) △H >0。该反应的化学平衡常数的表达式K= 。
2 NH3(g)+CO2(g) △H >0。该反应的化学平衡常数的表达式K= 。
关于该反应的下列说法正确的是
A.混合气体的平均相对分子质量不再改变,可以作为化学平衡到达的标志
B.在平衡体系中增加水的用量可使该反应的平衡常数增大
C.降低温度使CO(NH2)2的转化率增大
D.达到平衡后,再充入少量H2O,重新达到平衡,H2O的转化率会减小
(2)一定条件下,某密闭容器中充入等物质的量的NH3和CO2,发生反应:CO2(g) +2NH3(g) CO (NH2)2 (s) +H2O(g),混合气体中NH3的体积分数[φ(NH3)]随时间变化关系如图所示。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的体积分数[φ(NH3)]随时间变化关系如图所示。
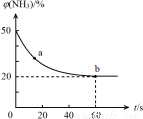
则a点的正反应速率V正(CO2)_________ b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________ 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学试卷(解析版) 题型:选择题
通过以下反应均可获取H2。下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g) ΔH2=131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g) ΔH3=206.1kJ·mol–1
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,ΔH3减小
D.反应CH4(g)=C(s)+2H2(g)的ΔH=74.8kJ·mol–1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:填空题
下图表示一些晶体中的某些结构,他们分别是氯化钠、氯化铯、干冰、金刚石、石墨结构中的某一种的某一部分(黑点可表示不同或相同的粒子)。
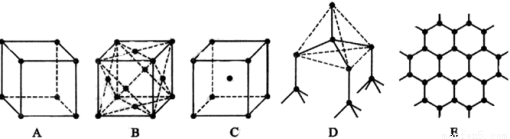
(1)其中代表金刚石的是 (填编号字母,下同),金刚石 中每个碳原子与 个碳原子最接近且距离相等。
中每个碳原子与 个碳原子最接近且距离相等。
(2)其中代表石墨的是 ,其中每个正六边形占有的碳原子数平均为____ 个;
(3)其中表示氯化钠的是 ,每个钠离子周围与它最接近且距离相等的钠离子有 个;
(4)代表氯化铯的是 ,每个铯离子与 个氯 离子紧邻;
离子紧邻;
(5)代表干冰的是 ,每个二氧化碳分子与 个二氧化碳分子紧邻;
(6)由Mg、C、Ni三种元素形成的一种具有超导性的晶体,晶胞如图2所示。Mg位于C 和Ni原子紧密堆积所形成的空隙当中。与一个Ni原子距离最近的Ni原子的数目为 ,该晶体的化学式为 。


(图2) (图3)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上11月考试化学卷(解析版) 题型:填空题
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其原理是____________________(用离子方程式说明)。
(2)相同条件下,0.1 mol·L-1 NH4Al(SO4)2 溶液中 c(NH4+)________(填“等于”、“大于”或“小于”)0.1 mol·L-1 NH4HSO4溶液中 c(NH4+)。
(3)均为 0.1 mol·L-1 的几种电解质溶液的pH 随温度变化的曲线如下图1所示。
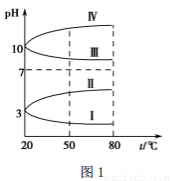
①其中符合0.1 mol·L-1 NH4Al(SO4)2溶液的pH随温度变化的曲线是________(填罗马数字),导致 NH4Al(SO4)2溶液的pH 随温度变化的原因是_____________________;
②20 ℃时,0.1 mol·L-1 NH4Al(SO4)2溶液中 2c(SO42-)-c(NH4+)-3c(Al3+)=____________ mol·L-1。
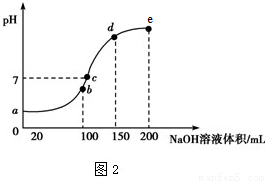
(4)室温时,向100 mL 0.1 mol·L-1 NH4HSO4溶液中滴加 0.1 mol·L-1 NaOH溶液,溶液pH与NaOH溶液体积的关系曲线如上图2所示。
试分析图中 a、b、c、d四个点,水的电离程度最大的是___________点,在b点,溶液中各离子浓度由大到小的排列顺序是_____________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上11月考试化学卷(解析版) 题型:选择题
某温度下,在2 L的密闭容器中,加入1 mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g) 3Z(g)平衡时, X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1mol Z(g),再次达到平衡后,X、Y、 Z的体积分数不变。下列叙述不正确的是( )
3Z(g)平衡时, X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1mol Z(g),再次达到平衡后,X、Y、 Z的体积分数不变。下列叙述不正确的是( )
A.m=2 B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为 1∶1 D.第二次平衡时,Z的浓度为 0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三上第四次月考化学卷(解析版) 题型:选择题
如图2所示,β-紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。下列说法正确的是
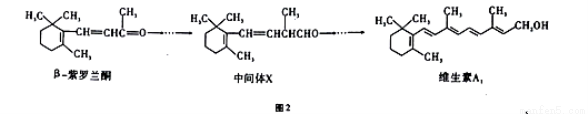
A.β-紫罗兰酮的分子式为C13H22O
B.1mol中间体X 最多能与2molBr2发生加成反应
C.维生素A1难溶于CCl4溶液
D.β-紫罗兰酮与中间体X互为同分异构体
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练三化学试卷(解析版) 题型:选择题
室温下,甲、乙两烧杯均盛有5mLpH=11的某一元碱溶液,向乙烧杯中加水稀释至pH=10。关于甲、乙两烧杯中溶液的描述不正确的是( )
A.溶液的体积:10V甲≤V乙
B.水电离出的OH-浓度:10c(H+)甲=c(H+)乙
C.若分别用等浓度的HCl溶液完全中和,所得溶液的PH:甲≤乙
D.若分别与5mLpH=3的HCl溶液反应,所得溶液的pH:甲≤乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com