��������1�����ø�˹���ɷ�����
��2������ͼ��֪��ߵ㷴Ӧ����ƽ�⣬����ƽ����¶�Խ�ߣ��գ�CH
3OH��ԽС������ƽ�����淴Ӧ���У��ݴ��жϣ�
��A���ٳ���1mol CO
2��3mol H
2���ɵ�ЧΪ��ʼ�����Ϊԭ����2��������2mol CO
2��6mol H
2��ƽ����ٽ����ѹ��Ϊԭ�������������ѹǿƽ���������С�ķ����ƶ�����������Ӧ�ƶ�����Ӧ���ת��������
B������v=
����v��H
2���жϣ�
C������ת���ʵĶ�������жϣ�
D�����¶��¸÷�Ӧ��K=
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
���������ݼ��㣻
E���÷�ӦΪ���ȷ�Ӧ�������¶�ƽ�����淴Ӧ���У�n��CH
3OH������n��CO
2������
��3�����ݷ�Ӧ������������غ�ķ�����д��ѧ����ʽ��
��4������ͼʾ֪��Ag-Pt�缫��NO
3-������ԭ��Ӧ�����Ag-Pt�缫Ϊ��������BΪ������AΪ��Դ��������������Ӧ��NO
3-�õ��ӷ�����ԭ��Ӧ����N
2�����õ���غ���ԭ���غ�֪�������Ӳ��뷴Ӧ����ˮ���ɣ�
��ת��2mol����ʱ��������������ӦΪH
2Oʧ��������ΪO
2��H
+������1molˮ������2molH
+���������ң���������������18g���������зų�0.2molN
2��5.6g����ͬʱ��2molH
+��2g�����������ң�
���
�⣺��1����֪��CH
4��g��+4NO
2��g��=4NO��g��+CO
2��g��+2H
2O��g����H
1=-574kJ?mol
-1 CH
4��g��+4NO��g��=2N
2��g��+CO
2��g��+2H
2O��g����H
2=-1160kJ?mol
-1���ܻ�ѧ��Ӧ��һ����ɻ��Ƿּ�����ɣ��䷴Ӧ������ͬ�ģ���ʽ��ӣ��ɵ�
2CH
4��g��+4NO
2��g��=2N
2��g��+2CO
2��g��+4H
2O��g����H=-1734 kJ/mol
��CH
4��g��+2NO
2��g��=N
2��g��+CO
2��g��+2H
2O��g����H=-867 kJ?mol
-1�ʴ�Ϊ��CH
4��g��+2NO
2��g��=N
2��g��+CO
2��g��+2H
2O��g����H=-867 kJ?mol
-1��
��2������ͼ��֪��ߵ㷴Ӧ����ƽ�⣬��ƽ����¶�Խ�ߣ��գ�CH
3OH��ԽС��˵�������¶�ƽ�����淴Ӧ���У������¶�ƽ�����ȷ�����У��淴ӦΪ���ȷ�Ӧ��������ӦΪ���ȷ�Ӧ������H
3��0���ʴ�Ϊ������
����ͼ2��֪����ʼ������̼��Ũ��Ϊ1.0mol/L����ʼ�����г���1mol CO
2��3mol H
2�����Կ�ʼ������Ũ��Ϊ3.0mol/L���������Ϊ
=1L��
ƽ��ʱ���״���Ũ��Ϊ0.75mol/L
CO
2��g��+3H
2��g��?CH
3OH��g��+H
2O��g��
��ʼ��mol/L����1 3 0 0
�仯��mol/L����0.75 2.25 0.75 0.75
ƽ�⣨mol/L����0.25 0.75 0.75 0.75
A��ͨ�����������֪������̼��ת����Ϊ
��100%=75%���ٳ���1mol CO
2��3mol H
2���ɵ�ЧΪ��ʼ�����Ϊԭ����2��������2mol CO
2��6mol H
2��ƽ����ٽ����ѹ��Ϊԭ�������������ѹǿƽ���������С�ķ����ƶ�����������Ӧ�ƶ�����Ӧ���ת�������������ٴδﵽƽ��ʱc��CH
3OH����1.5mol/L����A����
B��ͨ�����������֪������ת����Ϊ
��100%=75%����B��ȷ��
C��10�����ڣ�������ƽ����Ӧ����Ϊv��H
2��=
=0.225mol/��L?min������C����
D�����¶��¸÷�Ӧ��K=
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
=
=
����D����
E���÷�ӦΪ���ȷ�Ӧ�������¶�ƽ�����淴Ӧ���У�n��CH
3OH������n��CO
2����������
ֵ��С����E����
��ѡ��B��
��3�������е�SO
2��NO
2�����ʵ���֮��Ϊ1��1��һ�����İ�����������Ӧ����������狀�����淋Ļ������Ϊ����Ʒ���ʣ�����12NH
3+3O
2+4SO
2+4NO
2+6H
2O=4��NH
4��
2SO
4+4NH
4NO
3��
�ʴ�Ϊ��12NH
3+3O
2+4SO
2+4NO
2+6H
2O=4��NH
4��
2SO
4+4NH
4NO
3��
��4������ͼʾ֪��Ag-Pt�缫��NO
3-������ԭ��Ӧ�����Ag-Pt�缫Ϊ��������BΪ������AΪ��Դ��������������Ӧ��NO
3-�õ��ӷ�����ԭ��Ӧ����N
2�����õ���غ���ԭ���غ�֪��H
2O���뷴Ӧ����ˮ���ɣ�
���������Ϸ����ĵ缫��ӦʽΪ��2NO
3-+12H
++10e
-=N
2+6H
2O��
�ʴ�Ϊ��A��2NO
3-+12H
++10e
-=N
2+6H
2O��
��ת��2mol����ʱ��������������ӦΪH
2Oʧ��������ΪO
2��H
+������1molˮ������2molH
+���������ң���������������18g���������зų�0.2molN
2��5.6g����ͬʱ��2molH
+��2g�����������ң������������������3.6g����Ĥ������Һ�������仯���m��-��m�ң�=18g-3.6g=14.4g��ת��1mol���ӣ���Ĥ������Һ�������仯��7.2g��
�ʴ�Ϊ��7.2��





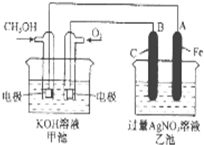 ��ͼ��һ����ѧ���̵�ʾ��ͼ����֪�׳ص��ܷ�ӦʽΪ��
��ͼ��һ����ѧ���̵�ʾ��ͼ����֪�׳ص��ܷ�ӦʽΪ��


 ʵʩ�Լ�����Դ�˷Ѻͽ��ͷ����ŷ�Ϊ�������ݵĽ��ܼ������ߣ���Ӧ��ȫ���������⡢������Դ��Լ�͡������Ѻ������ı�Ȼѡ������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����������ѧ֪ʶ������������⣺
ʵʩ�Լ�����Դ�˷Ѻͽ��ͷ����ŷ�Ϊ�������ݵĽ��ܼ������ߣ���Ӧ��ȫ���������⡢������Դ��Լ�͡������Ѻ������ı�Ȼѡ������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����������ѧ֪ʶ������������⣺
 ��֪�ס��ҡ�������4�����ʾ����г�������Ԫ��A�����м�Ϊ����ɫ��ĩ������֮������ͼ��ʾ��ת����ϵ��ת�������в��ֲ���δ�����
��֪�ס��ҡ�������4�����ʾ����г�������Ԫ��A�����м�Ϊ����ɫ��ĩ������֮������ͼ��ʾ��ת����ϵ��ת�������в��ֲ���δ�����