
| 乙醇 |


 ,H为
,H为 ,I为
,I为 ,F为
,F为 ,E为
,E为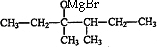 ,D为
,D为 ,C为
,C为 ,B为
,B为 ,A为
,A为 ,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为:
,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为: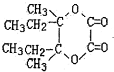 ,结合有机物的结构和性质以及题目要求可解答该题.
,结合有机物的结构和性质以及题目要求可解答该题. ,H为
,H为 ,I为
,I为 ,F为
,F为 ,E为
,E为 ,D为
,D为 ,C为
,C为 ,B为
,B为 ,A为
,A为 ,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为:
,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为: ,
, ,用系统命名法命名为:2-丁醇,故答案为:2-丁醇;
,用系统命名法命名为:2-丁醇,故答案为:2-丁醇; 和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,故答案为:HOOC-COOH;
和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,故答案为:HOOC-COOH; +O2
+O2| Cu |
| △ |
 +2H2O;
+2H2O; ,
, +O2
+O2| Cu |
| △ |
 +2H2O;
+2H2O; ;
; ,D的同分异构体符合以下条件:①能与Na反应反出H2,说明含有-OH;③有二种官能团,还含有碳碳双键;②核磁共振氢谱有四组峰,分子中有4种化学环境不同的H原子,且羟基不能与碳碳双键中的碳原子直接相连,符合条件的同分异构体为:CH2=C(CH3)CH2OH,
,D的同分异构体符合以下条件:①能与Na反应反出H2,说明含有-OH;③有二种官能团,还含有碳碳双键;②核磁共振氢谱有四组峰,分子中有4种化学环境不同的H原子,且羟基不能与碳碳双键中的碳原子直接相连,符合条件的同分异构体为:CH2=C(CH3)CH2OH,

 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
| A、苯乙烯分子中所有原子可能在同一个平面上 |
| B、分子式为C7H8O且分子中有苯环有机物共有4种 |
| C、乙醇和甘油互为同系物 |
| D、除去乙醇中混有的甲烷,可将混合气体通过酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 ,合成路线如下
,合成路线如下
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 3 |
| 16 |
| n(CH3OH) |
| n(CO2) |
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaH2能与水反应生成H2,可用作野外制氢气 |
| B、NH3具有还原性,可与灼热的CuO反应制备少量氮气 |
| C、SO2具有还原性,可使酸性高锰酸钾溶液褪色 |
| D、Si能导电,可用于制作光导纤维 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com