
【题目】下列措施不合理的是( )
A.将煤粉碎,增大固体的表面积可以有效加快煤燃烧的速率
B.空气过量有利于煤充分燃烧,因此鼓入空气的量越多约好
C.可以用在煤中加入生石灰,减少SO2气体的排放
D.煤的气化可以使煤发生化学反应转化为水煤气等
【答案】B
【解析】解:A.将煤粉碎,可以增大固体的表面积,从而能够有效加快煤燃烧的速率,故A正确; B.通入空气的量过大、空气的量过多会带走热量,所以一般是通入适当过量的空气,故B错误;
C.生石灰可与二氧化硫反应生成亚硫酸钙,最终被氧化为硫酸钙,减少二氧化硫的排放,减少环境污染,故C正确;
D.煤的气化的化学反应方程式:C(s)+H2O(g) ![]() CO(g)+H2(g),煤的气化可以使煤发生化学反应转化为水煤气,故D正确;
CO(g)+H2(g),煤的气化可以使煤发生化学反应转化为水煤气,故D正确;
故选B.
【考点精析】解答此题的关键在于理解物理变化与化学变化的区别与联系的相关知识,掌握化学变化本质:旧键断裂、新键生成或转移电子等;二者的区别是:前者无新物质生成,仅是物质形态、状态的变化,以及对二氧化硫的污染及治理的理解,了解SO2是污染大气的主要有害物质之一,直接危害是引起呼吸道疾病;形成酸雨pH<5、6,破坏农作物、森林、草原、使土壤酸性增强等等;含SO2的工业废气必须经过净化处理才能排放到空气中.


科目:高中化学 来源: 题型:
【题目】已知溶液中可发生反应:2FeBr2+Br2=2FeBr3 , 现向100mL的FeBr2溶液中通入3.36LCl2(标准状况),充分反应后测得溶液中Cl﹣和Br﹣ 的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为( )
A.2molL﹣1
B.1molL﹣1
C.0.4molL﹣1
D.0.2molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol碳完全燃烧后可放出393.5KJ的热量,下列热化学方程式正确的是( )
A.C(s)+O2(g)=CO2(g)△H=+393.5 kJ/mol
B.C(s)+ ![]() O2(g)=CO(g)△H=﹣393.5 kJ/mol
O2(g)=CO(g)△H=﹣393.5 kJ/mol
C.C+O2=CO2△H=﹣393.5 kJ/mol
D.C(s)+O2(g)=CO2(g)△H=﹣393.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离提纯方法不正确的是 ( )
A.分离KNO3和氯化钠,常用结晶与重结晶B.提纯含有碘的食盐,常用升华法
C.去除乙醇中的水分离常用蒸馏法D.苯和酸性高锰酸钾溶液可用分液法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向氯水中加入下列物质,表中各项均正确的是( )
选项 | 加入物质 | 现象 | 解释或离子方程式 |
A | AgNO3溶液 | 有白色沉淀生成 | Cl﹣+Ag+═AgCl↓ |
B | 石蕊试液 | 显红色 | 氯水中有盐酸、次氯酸 |
C | CaCO3 | 有气体放出 | CO |
D | FeCl2和KSCN溶液 | 有红色沉淀生成 | 2Fe2++Cl2═2Fe3++2Cl﹣ |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用粗盐(含Ca2+、Mg2+、SO42﹣等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示.下列有关说法正确的是 ( ) 
A.对粗盐溶液除杂可依次加入NaOH,Na2CO3、BaCl2 , 再加入盐酸调节溶液pH
B.饱和食盐水中先通入的气体为CO2
C.流程图中的系列操作中一定需要玻璃棒
D.
如图所示装置可以比较Na2CO3和NaHCO3晶体的热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯( ![]() )的下列叙述中:①能使酸性KMnO4溶液褪色;②可发生加聚反应;③可溶于水;④可溶于苯;⑤能发生硝化反应;⑥所有的原子可能共平面.其中正确的是( )
)的下列叙述中:①能使酸性KMnO4溶液褪色;②可发生加聚反应;③可溶于水;④可溶于苯;⑤能发生硝化反应;⑥所有的原子可能共平面.其中正确的是( )
A.①②③④⑤
B.①②⑤⑥
C.①②④⑤⑥
D.全部正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.回答有关问题:
(1)从能量的角度看,断开化学键要 , 形成化学键要
(2)已知拆开1molH﹣H键、1molI﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ.则由氢气和碘反应生成1mol HI需要(填“放出”或“吸收”)kJ的热量.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示: 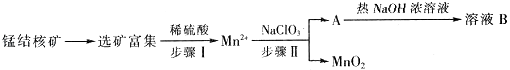
部分难溶的电解质溶度积常数(Ksp)如下表:
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10﹣17 | 10﹣17 | 10﹣39 |
已知:一定条件下,MnO4﹣可与Mn2+反应生成MnO2
(1)步骤Ⅱ中消耗0.5molMn2+时,用去1molL﹣1的NaClO3溶液200ml,该反应离子方程式为 .
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是 .
(3)MnO2是碱性锌锰电池的正极材料.放电过程产生MnOOH,该电池正极的电极反应式是 . 如果维持电流强度为5A,电池工作五分钟,理论消耗锌g.(已知F=96500C/mol)
(4)向废旧锌锰电池内的混合物(主要成分MnOOH、Zn(OH)2)中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的离子方程式 . 向所得溶液中滴加高锰酸钾溶液产生黑色沉淀,设计实验证明黑色沉淀成分为MnO2
(5)用废电池的锌皮制作ZnSO47H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加入稀H2SO4和H2O2 , 铁溶解变为Fe3+ , 加碱调节pH为时,铁刚好沉淀完全(离子浓度小于1×10﹣5molL﹣1时,即可认为该离子沉淀完全).继续加碱调节pH为时,锌开始沉淀(假定Zn2+浓度为0.1molL﹣1).若上述过程不加H2O2 , 其后果和原因是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com