
【题目】已知溶液中可发生反应:2FeBr2+Br2=2FeBr3 , 现向100mL的FeBr2溶液中通入3.36LCl2(标准状况),充分反应后测得溶液中Cl﹣和Br﹣ 的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为( )
A.2molL﹣1
B.1molL﹣1
C.0.4molL﹣1
D.0.2molL﹣1
【答案】A
【解析】解:还原性Fe2+>Br﹣ , 所以通入氯气先发生反应2Fe2++Cl2═2Fe3++2Cl﹣ , Fe2+反应完毕,剩余的氯气再反应反应2Br﹣+Cl2═Br2+2Cl﹣ , 溶液中含有Br﹣ , 说明氯气完全反应,Cl2的物质的量= ![]() =0.15mol,若Br﹣没有反应,则c(FeBr2)=0.5n(Br﹣)=0.15mol,0.15molFe2+只能消耗0.075mol的Cl2 , 故有部分Br﹣参加反应,
=0.15mol,若Br﹣没有反应,则c(FeBr2)=0.5n(Br﹣)=0.15mol,0.15molFe2+只能消耗0.075mol的Cl2 , 故有部分Br﹣参加反应,
设FeBr2的物质的量为x,则n(Fe2+)=x mol,n(Br﹣)=2x mol,未反应的n(Br﹣)=0.3 mol,参加反应的n(Br﹣)=(2x﹣0.3)mol,根据电子转移守恒有x×1+[2x﹣0.3]×1=0.15mol×2,解得x=0.2 mol,所以原FeBr2溶液的物质的量浓度为 ![]() =2mol/L.
=2mol/L.
故选:A.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO33H2O.实验过程如图1: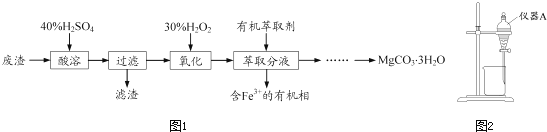
(1)酸溶过程中主要反应的热化学方程式为
MgCO3(S)+2H+(aq)═Mg2+(aq)+CO2(g)+H2O(l)△H=﹣50.4kJmol﹣1
Mg2SiO4(s)+4H+(aq)═2Mg2+(aq)+H2SiO3(s)+H2O(l)△H=﹣225.4kJmol﹣1
酸溶需加热的目的是;所加H2SO4不宜过量太多的原因是 .
(2)加入H2O2氧化时发生发应的离子方程式为 .
(3)用图2所示的实验装置进行萃取分液,以除去溶液中的Fe3+ .
①实验装置图中仪器A的名称为 .
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂,、静置、分液,并重复多次.
(4)请补充完整由萃取后得到的水溶液制备MgCO33H2O的实验方案:边搅拌边向溶液中滴加氨水, , 过滤、用水洗涤固体2﹣3次,在50℃下干燥,得到MgCO33H2O.
[已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香花石由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2 , X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍.下列说法正确的是( )
A.气态氢化物的沸点:W<T<R
B.离子半径:T﹣>R2﹣
C.最高价氧化物对应的水化物碱性:Y>X
D.XR2、WR2两化合物含有的化学键的类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,甲、乙、丙分别表示在不同条件下可逆反应:A(g)+B(g)xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系.
请根据图象回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则曲线表示无催化剂时的情况(填字母,下同);
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性气体后的情况,则曲线表示恒温恒容的情况;
(3)根据丙图可以判断该可逆反应的正反应是热反应(填“吸”或“放”),计量数x的值(填取值范围);判断的依据分别是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2和SO2都能使品红溶液褪色。若将等物质的量的Cl2、SO2混合后,再通入品红与BaCl2的混合溶液,能观察到的现象是①溶液很快褪色②溶液不褪色 ③出现沉淀④不出现沉淀
A. ①② B. ①③ C. ②③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.按系统命名法,  的名称为2﹣甲基﹣3,5﹣二乙基己烷
的名称为2﹣甲基﹣3,5﹣二乙基己烷
B.用Na2CO3溶液能区分CH3COOH、CH3CH2OH、苯和硝基苯四种物质
C.等质量的甲烷、乙烯、1,3一丁二烯分别充分燃烧,所消耗氧气的量依次增加
D.葡萄糖、蔗糖、油脂和蛋白质在一定条件下都能水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O
将2.56g铜放入14mL浓硝酸中,随着铜的不断减少,反应生成的气体颜色逐渐变浅.当铜片完全消失时,收集到干燥的NO、NO2混合气体,换算成标准状况下体积为1.344L(忽略气体的溶解及转化).请回答下列问题:
(1)反应中被还原的HNO3的物质的量是mol.
(2)生成气体中NO与NO2的体积比是
(3)该浓HNO3的物质的量浓度≥molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类1000年的能源需要.天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O分子.若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为( )
A.CH4?14H2O
B.CH4?8H2O
C.CH4? ![]() H2O
H2O
D.CH4?6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施不合理的是( )
A.将煤粉碎,增大固体的表面积可以有效加快煤燃烧的速率
B.空气过量有利于煤充分燃烧,因此鼓入空气的量越多约好
C.可以用在煤中加入生石灰,减少SO2气体的排放
D.煤的气化可以使煤发生化学反应转化为水煤气等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com