
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如下,总反应:
2Cu+H2O![]() Cu2O+H2
Cu2O+H2![]() 。下列说法正确的是
。下列说法正确的是

A. 石墨电极发生氧化反应
B. 铜电极发生的电极反应式:2Cu-2e- + H2O==Cu2O+2H+
C. 电解后溶液的PH减小
D. 当有0.1mol电子转移时,有0.05 molCu2O生成。
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如表:
元素 | 相关信息 |
X | X的基态原子L层电子数是K层电子数的2倍 |
Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
Z | Z是第三周期电负性最大的元素 |
W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)W位于元素周期表第周期第族,其基态原子最外层有个电子 .
(2)X的电负性比Y的(填“大”或“小”),XY2的价层电子对模型为 .
(3)X和Y的简单气态氢化物中,较稳定的是 , 沸点较高的是(写化学式) .
(4)化合物XYZ2中σ键和π键个数比为 .
(5)写出与W同周期且导电性强于W的某元素价电子排布式. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜品醇可作为消毒剂、抗氧化剂、医药和溶剂,其结构简式如图所示.下列说法正确的是( ) 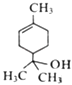
A.萜品醇的分子式为C9H10O
B.萜品醇能发生加成反应和取代反应
C.萜品醇能被高锰酸钾被和溴水氧化
D.1mol萜品醇最多与3mol H2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g)ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量QkJ。则下列分析正确的是
2SO3(g)ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量QkJ。则下列分析正确的是
A. 若反应开始时容器体积为2 L,则v(SO3)=0.35 mol·L-1·min-1
B. 2 min后,向容器中再通入一定量的SO3气体,重新达到平衡时,SO2的含量降低
C. 若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO3)大于1.4 mol
D. 若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于QkJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,在容积不变的密闭容器中将N2和H2混合,使其在一定条件下发生反应:N2(g)+3H2(g)2HN3(g),并达到化学平衡,根据表中数据回答有关问题
物质的量浓度 | N2 | H2 | NH3 |
起始/molL﹣1 | a | 6 | 0 |
转化/molL﹣1 | b | c | d |
平衡/molL﹣1 | 1 | e | 3 |
(1)表中a= , e=
(2)若反应经3min达到平衡,则反应速率v(N2)=molL﹣1min﹣1;
(3)该反应体系的起始状态与平衡状态的压强之比为;
(4)上述反应过程中,如果降低温度,则反应速度(填“增大”或“减小”“不变”).
(5)下列各项中,可以说明上述反应达到平衡的是(填序号)
A.混合气体的密度不再变化
B.混合气体的压强不再变化
C.N2的正反应速率等于逆反应速率
D.N2的浓度保持恒定不变.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)电动汽车上用的铅蓄电池是以一组充满海绵状态铜的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解液。放电时总反应为:Pb + PbO2 + 2H2SO4 = 2PbSO4 + 2H2O
① 写出放电时负极的电极反应式:______________________________;
② 铅蓄电池放电时,溶液的pH将_________(填增大、减小或不变)。当外电路上有0.5mol电子通过时,溶液中消耗H2SO4的物质的量为___________。
③ 放电完后,对该电池进行充电,在连接电源的负极一端生成________。(填“Pb”或“PbO2”)
(2)下图是某宇宙飞船中使用的氢氧燃料电池。其导电介质为KOH,总反应为:2H2 + O2=2H2O。
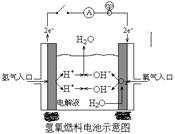
① 则负极通入的是_______,(填“H2”或“O2”)负极电极反应式为:_______________________,正极电极反应式为:______________________。
②如把导电介质改为稀H2SO4,则电极反应式为:负极__________________,正极______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过下列两步实验测定草酸晶体(H2C2O4·xH2O)中结晶水x的值:
①称取2.52 g草酸晶体,配制成100 .00 mL溶液。
②取25.00 mL所配溶液置于锥形瓶中,加入适量稀硫酸后,用浓度为0.100 mol·L-1 KMnO4溶液进行滴定。其反应原理是:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
请回答下列问题:
(1)实验②中,KMnO4应装在______滴定管中(填“酸式”、“碱式”)。
(2)如图表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积______。
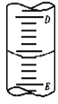
A.是amL B.是(50-a)mL
C.一定大于amL D.一定大于(50-a)mL
(3)判断达到滴定终点的现象是_____________________________;
若滴定终点时,共用去KMnO4溶液20.00 mL,则x =__________。
(4)若在滴入KMnO4溶液之前滴定管的尖嘴部分有气泡,滴定结束后气泡消失,则会使测定结果______(偏高、偏低或无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国外试行用“汽水”(碳酸饮料)浇灌植物,它的作用是( )
①对植物的呼吸作用有利。② 改良碱性土壤,调节pH值。③有利于土壤中钙离子、镁离子被植物吸收。④加速光合作用的进行。其中 ( )
A.只有②③④正确
B.只有②④正确
C.只有②正确
D.全部正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com