
【题目】H2R是一种二元弱酸。25℃时,向H2R溶液中逐滴加入NaOH溶液,混合溶液中lgX[X为![]() 或
或![]() ]与pH的变化关系如图所示。下列说法一定正确的是
]与pH的变化关系如图所示。下列说法一定正确的是

A. Ⅱ表示lg![]() 与pH的变化关系
与pH的变化关系
B. pH=1.22的溶液中:2c(R2-)+c(HR-)<c(Na+)
C. NaHR溶液中c(H+)>c(OH-)
D. 当溶液呈中性时:c(Na+)>c(HR-)>c(R2-)>c(H+)=c(OH-)
【答案】C
【解析】
二元弱酸H2R的K1=![]() >K2=
>K2=![]() ,当溶液的pH相同时,c(H+)相同,可以看出lgX:Ⅰ>Ⅱ,则Ⅰ表示lg
,当溶液的pH相同时,c(H+)相同,可以看出lgX:Ⅰ>Ⅱ,则Ⅰ表示lg![]() 与pH的变化关系,Ⅱ表示lg
与pH的变化关系,Ⅱ表示lg![]() 与pH的变化关系,据此分析作答。
与pH的变化关系,据此分析作答。
根据上述分析可知,
A.Ⅱ表示lg![]() 与pH的变化关系,A项错误;
与pH的变化关系,A项错误;
B. pH=1.22时,溶液呈酸性,则c(H+)>c(OH),根据电荷守恒c(Na+)+c(H+)=c(HR-)+2c(R2-)+c(OH)可知,2c(R2-) + c(HR-)>c(Na+),B项错误;
C. 二元弱酸H2R的K1=![]() ,则当pH=1.22时,lg
,则当pH=1.22时,lg![]() =0,即
=0,即![]() =1,可知第一步电离平衡常数K1=10-1.22,则HR-的水解平衡常数Kh=
=1,可知第一步电离平衡常数K1=10-1.22,则HR-的水解平衡常数Kh=![]() ,同理根据电离平衡常数的定义可知,当pH=4.19时,曲线Ⅱ中lg
,同理根据电离平衡常数的定义可知,当pH=4.19时,曲线Ⅱ中lg![]() =0,即
=0,即![]() =1,得出第二步电离平衡常数K2=10-4.19 > Kh,由此可知NaHR溶液中HR-的电离程度大于水解程度,即c(H+) > c(OH-),C项正确;
=1,得出第二步电离平衡常数K2=10-4.19 > Kh,由此可知NaHR溶液中HR-的电离程度大于水解程度,即c(H+) > c(OH-),C项正确;
D. 曲线中lgX随pH值的增大而增大,则根据图像性质可推出,曲线Ⅱ在pH=7(中性)时,推知lg![]() > 1,即c(R2-) > c(HR-),D项错误;
> 1,即c(R2-) > c(HR-),D项错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】50℃时,0.1mol·L-1Na2CO3溶液pH=12,下列判断正确的是
A. c(OH-)=10-2mol·L-1
B. 加入少量NaOH固体,c(Na+)和c(CO32-)均增大
C. c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
D. 2c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
A. 该溶液的pH=4 B. 升高温度,溶液的pH增大 C. 此酸的电离平衡常数约为1×10-7 D. 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质在水溶液中存在各种行为,如电离、水解、沉淀溶解等,据所学知识回答下列问题:
(1)t℃时,纯水中c(H+)=1×10-6 mol·L-1,则该温度下水的离子积常数KW=_______mol2L-2;该温度下,pH=2的H2SO4溶液中由水电离出的[H+]为_________ molL-1。
(2)25℃时,相同物质的量浓度的下列溶液中:①NaCl ②NaOH ③H2SO4 ④(NH4)2SO4,其中水的电离程度由大到小顺序为__________________(用序号回答)。
(3)25℃时,将 a mol·L-1 的醋酸和 b mol·L-1 的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中c(CH3COO-)+c(CH3COOH)=______ molL-1,a____ b(填“﹥”、“﹤”或“=”)。
(4)常温下,稀释0.5 mol·L1的醋酸溶液,下图中的纵坐标不能表示_________

A.CH3COOH的电离程度 B.溶液中H+的数目
C.溶液中![]() 的值 D.溶液中CH3COOH的浓度
的值 D.溶液中CH3COOH的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电致变色玻璃以其优异的性能将成为市场的新宠。如图所示为五层膜的玻璃电致变色系统,其工作原理是:在外接电源下,通过在膜材料内部发生氧化还原反应,实现对器件的光透过率进行多级可逆性调节。(已知:WO3和Li4Fe4[Fe(CN)6]3均为无色透明,LiWO3和Fe4[Fe(CN)6]3均为蓝色)下列有关说法正确的是

A. 当B外接电源负极时,膜由无色变为蓝色
B. 当B外接电源负极时,离子储存层发生反应为:Fe4[Fe(CN)6]3+4Li++4eˉ=Li4Fe4[Fe(CN)6]3
C. 当A接电源的负极时,此时Li+得到电子被还原
D. 当A接电源正极时,膜的透射率降低,可以有效阻挡阳光
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实可以用勒夏特列原理解释的是( )
A. 新制的氯水在光照条件下颜色变浅
B. 使用催化剂,提高合成氨的产量
C. 高锰酸钾(KMnO4)溶液加水稀释后颜色变浅
D. H2、I2、HI平衡混合气体加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据热化学方程式N2(g)+3H2(g)![]() 2NH3(g)+92kJ,下列有关图像和叙述中正确的是
2NH3(g)+92kJ,下列有关图像和叙述中正确的是
A.  B.
B. 
C. 向密闭容器中通入1mol氮气和3mol氢气发生反应放出92kJ的热量D. 形成1mol氮氮键和3mol氢氢键所放出的能量比拆开6mol氮氢键所吸收的能量多92kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦炭是重要的工业原材料。
(1)已知在一定温度下,C(s)+CO2(g) ![]() 2CO(g) 平衡常数K1;C(s)+H2O(g)
2CO(g) 平衡常数K1;C(s)+H2O(g) ![]() CO(g)+H2(g) 平衡常数K2 ;CO(g)+H2O(g)
CO(g)+H2(g) 平衡常数K2 ;CO(g)+H2O(g) ![]() H2(g)+CO2(g) 平衡常数K。则K、K1、K2,之间的关系是__________。
H2(g)+CO2(g) 平衡常数K。则K、K1、K2,之间的关系是__________。
(2)用焦炭还原NO的反应为:2NO(g)+ C(s)![]() N2(g) + CO2(g) ΔH,向容积均为1L的甲、乙、丙三个恒温(反应温度分别为400℃、T ℃、400℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g) + CO2(g) ΔH,向容积均为1L的甲、乙、丙三个恒温(反应温度分别为400℃、T ℃、400℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
t/min | 0 | 40 | 80 | 120 | 160 |
n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(NO)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
n(NO)(丙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
①甲容器中,0~40 min内用NO的浓度变化表示的平均反应速率v(NO)=_____________ ;
②该反应的平衡常数表达式为__________________;400℃,该反应的平衡常数为_______;
③乙容器的反应温度T____400 ℃(填“>”“<”或“=”)
④丙容器达到平衡时,NO的转化率为___________;平衡时CO2的浓度为________。
⑤在恒容密闭容器中加入焦炭并充入NO气体,下列图像正确且能说明反应达到平衡状态的是___。
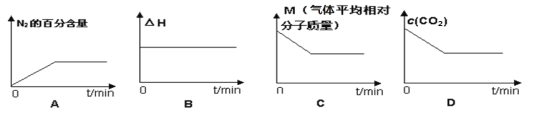
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得0.01mol/L的KMnO4的硫酸溶液和0.1mol/L的H2C2O4溶液等体积混合后,反应速率υ[mol/(L · s)]与反应时间t(s)的关系如图所示。该反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4==K2SO4+2MnSO4+10CO2↑+8H2O
回答如下问题:

(1)0→t2时间段内反应速率增大的原因是: _________________________________ ,
(2)t2→t时间段内反应速率减小的原因是: _______________ ,
(3)图中阴影部分“面积”表示t1→t3时间里________ 。
A.Mn2+物质的量浓度的增大 B.Mn2+物质的量的增加
C.SO42-物质的量浓度 D.MnO4-物质的量浓度的减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com