
【题目】海水的综合利用可以制备金属镁,其流程如图所示:
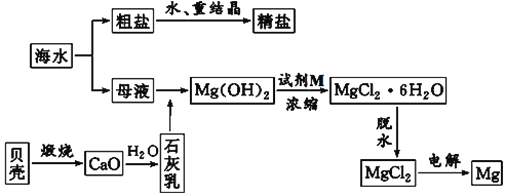
(1)海水提取镁要用到海滩上的贝壳,贝壳煅烧过程中发生反应的化学方程式为___________________________________________。
(2)母液中加入石灰乳反应的离子方程式为______。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
溶解时:_____________________________,
过滤时:_____________________________,
蒸发时:_____________________________。
(4)除去粗盐溶液中含有的![]() 、
、![]() 、
、![]() ,可依次加入
,可依次加入![]() 溶液、NaOH溶液、________,最后加入_________调节pH至中性。
溶液、NaOH溶液、________,最后加入_________调节pH至中性。
(5)写出金属镁在空气中燃烧的化学方程式____________________________。
【答案】![]()
![]() 搅拌加速溶解 引流 搅拌防止因局部过热造成液滴或晶体飞溅
搅拌加速溶解 引流 搅拌防止因局部过热造成液滴或晶体飞溅 ![]() 溶液 盐酸
溶液 盐酸 ![]()
【解析】
海水蒸发得到粗盐和母液,粗盐加入水溶解,重结晶得到精盐,母液中加入利用贝壳煅烧生成的氧化钙溶于水得到石灰乳,沉淀镁离子生成氢氧化镁沉淀,过滤得到沉淀中加入试剂M名称是盐酸溶解,蒸发浓缩,冷却结晶得到氯化镁晶体,在氯化氢中受热分解脱水得到氯化镁固体,通电电解熔融氯化镁生成镁和氯气;(1)贝壳的主要成分是CaCO3,煅烧分解生成氧化钙和二氧化碳;(2)母液中加入石灰乳反应生成氢氧化镁沉淀;(3)玻璃棒有搅拌、引流等作用;(4)把杂质转化为沉淀或气体除去,除钙离子用碳酸根,除镁离子用氢氧根,除硫酸根用钡离子。要注意除杂质的顺序,后加的试剂最好能把前面先加是过量试剂除掉;(5)镁在空气中燃烧生成氧化镁。
海水蒸发得到粗盐和母液,粗盐加入水溶解,重结晶得到精盐,母液中加入利用贝壳煅烧生成的氧化钙溶于水得到石灰乳,沉淀镁离子生成氢氧化镁沉淀,过滤得到沉淀中加入盐酸溶解,蒸发浓缩,冷却结晶得到氯化镁晶体,在氯化氢中受热分解脱水得到氯化镁固体,通电电解熔融氯化镁生成镁和氯气;(1)贝壳的主要成分是CaCO3,煅烧分解生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3![]() CaO+CO2↑;(2)母液中加入石灰乳反应的离子方程式为:Ca(OH)2+Mg2+=Mg(OH)2+Ca2+;(3)玻璃棒有搅拌、引流等作用,实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发3个步骤的操作中都要用到玻璃棒,其中:溶解时用玻璃棒搅拌起到加速溶解的作用;过滤时用到玻璃棒是起到引流的作用;蒸发过程中需要用玻璃棒不断搅拌,防止因局部过热造成液滴或晶体飞溅;(4)除去粗盐中的可溶性杂质:Mg2+、Ca2+、SO42-时,可以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓;加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3,碳酸钠必须加在氯化钡之后,除去粗盐溶液中含有的Ca2+、Mg2+、SO42-,可依次加入BaCl2溶液、NaOH溶液、Na2CO3溶液、最后加入盐酸调节PH至中性;(5)镁燃烧生成氧化镁,金属镁在空气中燃烧的化学方程式为:
CaO+CO2↑;(2)母液中加入石灰乳反应的离子方程式为:Ca(OH)2+Mg2+=Mg(OH)2+Ca2+;(3)玻璃棒有搅拌、引流等作用,实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发3个步骤的操作中都要用到玻璃棒,其中:溶解时用玻璃棒搅拌起到加速溶解的作用;过滤时用到玻璃棒是起到引流的作用;蒸发过程中需要用玻璃棒不断搅拌,防止因局部过热造成液滴或晶体飞溅;(4)除去粗盐中的可溶性杂质:Mg2+、Ca2+、SO42-时,可以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓;加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3,碳酸钠必须加在氯化钡之后,除去粗盐溶液中含有的Ca2+、Mg2+、SO42-,可依次加入BaCl2溶液、NaOH溶液、Na2CO3溶液、最后加入盐酸调节PH至中性;(5)镁燃烧生成氧化镁,金属镁在空气中燃烧的化学方程式为:![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】析氢腐蚀和吸氧腐蚀的负极反应是( )
A. Fe-2e-=Fe2+B. 2H+ +2e-=H2↑C. O2+4e- +2H2O= 4OH-D. Fe-3e-=Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进行化学实验时应强化安全意识。下列做法正确的是( )
A.金属钠着火时使用泡沫灭火器灭火
B.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗
C.用试管加热碳酸氢钠固体时使试管口竖直向上
D.不慎将酒精灯碰翻,酒精在实验台上燃烧起来,应用湿抹布盖灭
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是( )


A. ①是其他条件一定时,反应速率随温度变化的图像,正反应ΔH<0
B. ②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C. ③是在有无催化剂存在下建立的平衡过程图像,a是使用催化剂时的曲线
D. ④是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL0.1molL-1NaOH溶液中加入0.1molL-1的一元酸HA溶液pH的变化曲线如图所示。下列说法正确的是( )

A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA) B. a、b两点所示溶液中水的电离程度相同
C. pH=7时,c(Na+)=c(A-)+c(HA) D. b点所示溶液中c(A-)>c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
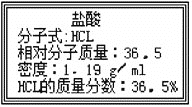
⑴该浓盐酸中HCL的物质的量浓度为 __________mol·L-1 。
⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是(____)
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
⑶某学生欲用上述浓盐酸和蒸馏水配制500ml物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取________ml上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
I.用量筒量取浓盐酸进俯视观察凹液面(______)
II.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水(______)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于合金的说法正确的是 ( )
①合金至少含两种金属
②合金中元素以化合物形式存在
③合金中一定含金属
④合金一定是混合物
⑤铁锈是一种铁合金
A.①②B.②③⑤C.③④D.③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲配制1mol/LNaOH溶液240ml,请回答:
(1)需称取NaOH固体____________g,用质量为23.1g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小___________(填字母),并在下图中选出能正确表示游码位置的选项_________(填字母)。

(2)选用的主要玻璃仪器除烧杯、玻璃棒外还有________________________。
(3)下列操作的顺序是(用序号表示)_________________。
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用天平准确称取所需的NaOH的质量,加入少量水,用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)下列情况对所配制的NaOH溶液浓度有何影响?(用“偏大”“偏小”“无影响”填写)
①容量瓶用蒸馏洗涤后残留有少量的水________________
②将热的溶液直接移入了容量瓶________________
③定容时,仰视容量瓶的刻度线________________
④转移溶液时,玻璃棒的下端在容量瓶的刻度线以上________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下进行反应,一段时间后测得反应前后各物质质量如表.该密闭容器中发生化学反应的基本类型可能是
物质 | X | Y | Z | Q |
反应前质量/g | 20 | 20 | 20 | 20 |
反应后质量/g | 20 | 30 | 16 | 14 |
A.分解反应B.置换反应C.复分解反应D.化合反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com