
【题目】常温下,用0.1molL-1HCl溶液滴定10.0mL浓度为0.1molL-1Na2CO3溶液,所得滴定曲线如图所示。下列微粒浓度大小关系正确的是
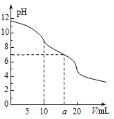
A.当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)
B.当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-)
C.当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
D.当V=a时:c(Na+)=c(Cl-)>c(H+)=c(OH-)
【答案】B
【解析】
试题分析:A.当V=0时为碳酸钠溶液,根据电荷守恒可知:c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(HCO3-),根据物料守恒可得:c(Na+)=2c(HCO3-)+2c(H2CO3)+2c(CO32-),根据电荷守恒和物料守恒可得:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-),故A错误;B.当V=5时,碳酸钠与氯化氢浓度相等,则氯离子的物质的量为总的碳原子的物质的量一半,根据物料守恒可得:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-),故B正确;C.当V=10时,此时恰好反应生成碳酸氢钠,碳酸氢钠溶液中碳酸氢根离子的水解大于其电离程度,则碳酸的浓度大于碳酸根离子,即c(CO32-)<c(H2CO3),正确的离子浓度大小关系为:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-),故C错误;D.v=a时,溶液为中性,c(H+)=c(OH-),根据电荷守恒可得:c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(Cl-)+c(HCO3-),则c(Na+)=2c(CO32-)+c(HCO3-)+c(Cl-),所以c(Na+)>c(Cl-)>c(H+)=c(OH-),故D错误;故选B。


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:
【题目】如图是研究二氧化硫性质的微型实验装置。现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气。下列说法中错误的是( )
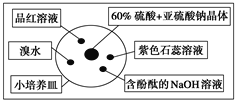
A. 紫色石蕊溶液变红色,说明SO2呈酸性
B. 品红溶液褪色,说明SO2具有漂白性
C. 溴水橙色褪去,体现了SO2的还原性
D. 含酚酞的NaOH溶液红色变浅,表明SO2能够和NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只用一种试剂,可区别Na2SO4、AlCl3、NH4Cl、MgSO4四种溶液,这种试剂是( )
A.HCl B.BaCl2 C.AgNO3 D.NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
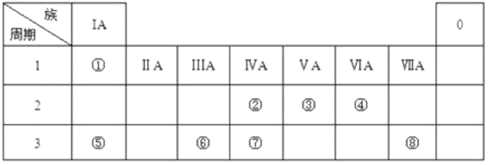
(1)地壳中含量最高的金属元素在周期表中的位置是 ;
(2)⑧形成的单质与水反应的离子方程式为 ;
(3)②⑦的非金属性强弱可通过比较这两种元素 (填编号)
a、原子的得电子能力
b、含氧酸的酸性
c、气态氢化物的稳定性
d、单质的熔点
(4)写出一种由④⑤⑧元素组成的既含离子键又含有共价键的物质的电子式 。
(5)化工行业最近合成了由②和③形成的化合物,其硬度比金刚石还大,该物质所形成的晶体还可能具有的性质或特点有 。(填编号)
①熔点很高 ②可以导电 ③不存在单个分子 ④具有空间网状结构
(6)①和③形成的某液态化合物摩尔质量与氧气相同,在常温常压下0.25mol该液态物质在足量的氧气中完全燃烧生成③的气态单质和液态水,同时放出QkJ的热量。写出该反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2气体是一种常用的消毒剂,我国从2 000年起逐步用ClO2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,在这个过程中,Fe2+、Mn2+的化合价升高,说明ClO2具有__________性。
(2)工业上可以通过下列方法制取ClO2,请完成该化学反应方程式:2KClO3+SO2=2ClO2+__________。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,是放热反应,当1molCl2参与反应时释放145kJ的热量,写出这个反应的热化学方程式:___________________。
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O![]() +I2=S4O
+I2=S4O![]() +2I-)
+2I-)
Ⅲ.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如下图所示:
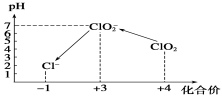
请回答:
①操作Ⅰ中反应的离子方程式是______________________。
②确定操作Ⅱ完全反应的现象是___________________。
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是____________________。
④若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是________mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1﹣氯丙烷跟NaOH的醇溶液共热,生成的产物再跟溴水反应,得到一种有机物,它的同分异构体有(除它之外)( )
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、请根据如下图所示转化关系回答有关问题。A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有强氧化性。
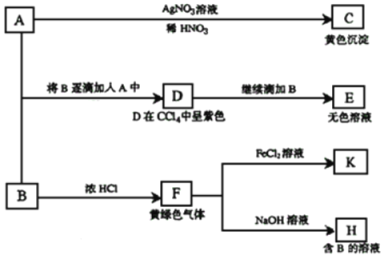
(1)写出A、B的化学式:A ,B 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式: , 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式: 。
II、(1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。在如下图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图像。

(2)将18.4gNaOH和NaHCO3固体混合物,在密闭容器中加热到约250℃,经充分反应后排出气体,冷却,称得剩余固体质量为16.6g。试计算混合物中NaOH的质量分数。(请写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、关于工业转化图(见下图):

1、①反应类型: ④反应类型: 。
2、实验室制备乙烯的反应条件是 ;反应温度过低会产生副产物: (写结构简式);
II、现拟分离混有乙醇、乙酸和水的乙酸乙酯粗产品,下图是分离操作步骤的流程图,试填写图中试剂的化学式及分离方法

(1)试剂b是 ;
(2)分离方法①是: ;分离方法②是: ;
(3)A是: ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com