
| A、C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
| B、C(C1-)=C(NH4+),且C(H+)═C(OH-) |
| C、C(NH4+)<C(Cl-)<C(H+)<C(OH-) |
| D、C(OH-)<C(NH4+)<C(H+)<C(Cl-) |


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
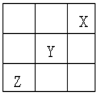 (1)根据氢元素最高正价最低负价的绝对值相等,有人提议把氢元素放在周期表中的ⅣA族.那么根据NaH的存在,又可把氢元素放在
(1)根据氢元素最高正价最低负价的绝对值相等,有人提议把氢元素放在周期表中的ⅣA族.那么根据NaH的存在,又可把氢元素放在查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al2(SO4)3═2Al3++3SO42- |
| B、NaHCO3═Na++H++CO32- |
| C、CH3COOH═CH3COO-+H+ |
| D、Na2CO3═Na2++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、20℃,10 mL 0.1mol?L-1硫酸 |
| B、20℃,5 mL 0.1 mol?L-1硫酸和5 mL水 |
| C、30℃,10 mL 1 mol?L-1硫酸 |
| D、30℃,5 mL 1 mol?L-1硫酸和5 mL水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
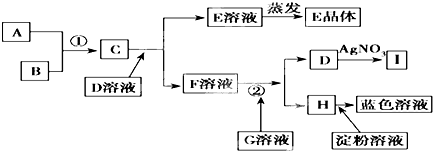
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量的铜与浓硝酸反应可生成NO |
| B、Fe在O2中的燃烧产物可用于制红色涂料 |
| C、Na、Cu可以分别用电解冶炼法、热还原法得到 |
| D、Fe2+、SO2都能使酸性高锰酸钾溶液褪色,前者表现出还原性后者表现出漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.20 | 20.22 | |
| 第二次 | 25.00 | 0.56 | 24.54 | |
| 第三次 | 25.00 | 0.42 | 20.40 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 |
| B、废旧电池不能随意丢弃,要进行深埋处理,防止重金属污染 |
| C、Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
| D、据测定,许多反应的温度每升高10℃,其反应速率增加2~4倍.在实验室或工业生产中,常采用加热的方法使化学反应在较高的温度下进行,以提高反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com