
| A、过量的铜与浓硝酸反应可生成NO |
| B、Fe在O2中的燃烧产物可用于制红色涂料 |
| C、Na、Cu可以分别用电解冶炼法、热还原法得到 |
| D、Fe2+、SO2都能使酸性高锰酸钾溶液褪色,前者表现出还原性后者表现出漂白性 |


科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
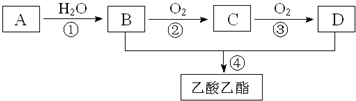
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
| A、1.6 mol |
| B、1.2 mol |
| C、大于1.6 mol |
| D、小于1.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
| B、C(C1-)=C(NH4+),且C(H+)═C(OH-) |
| C、C(NH4+)<C(Cl-)<C(H+)<C(OH-) |
| D、C(OH-)<C(NH4+)<C(H+)<C(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阴离子 | SO42-、NO2-、Cl- |
| 阳离子 | Fe2+、Fe3+、NH4-、Mg2+、Al2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称量时NaOH已经潮解 |
| B、向容量瓶中转移溶液时,容量瓶事先用蒸馏水洗涤过 |
| C、定容时俯视容量瓶的刻度线 |
| D、定容摇匀后,有少量溶液外流 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com