
能将分别含有Cu2+、Fe3+、Al3+、Fe2+、Mg2+、NH、Na+等离子的七种溶液一次鉴别出来的试剂是
A.NaHCO3溶液 B.NaOH溶液
C.KSCN溶液 D.NH3·H2O溶液
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:2016届辽宁省高三上学期一模化学试卷(解析版) 题型:选择题
下面是溶解性表中的部分内容(室温下测定):
阳离子 | 阴离子 | ||
OH- | SO42- | SO32- | |
Ca2+ | ① | 微 | 不 |
Fe3+ | 不 | 溶 | ② |
Cu2+ | 不 | ③ | 不 |
下列有关说法中正确的是
A.①处物质属于可溶性碱
B.②处物质组成为Fe2(SO3)3
C.③处物质为硫酸盐或者铜盐
D.①、③处物质在溶液中发生的反应一定是Cu2++2OH-===Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北大附中河南分校高二上9月考化学试卷(解析版) 题型:填空题
如图所示3套实验装置,分别回答下列问题:
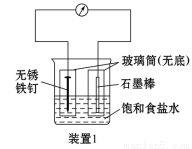
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入KSCN溶液呈无色,再滴入氯水即可观察到铁钉附近的溶液变红色,表明铁被_______;向插入碳棒的玻璃筒内滴入酚酞试液,可观察到碳棒附近的溶液变红,该电极反应为_______________。
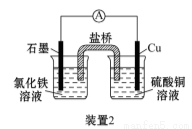
(2)装置2中的石墨是_________极(填“正”或“负”),该装置发生的总反应的离子方程式为__________。
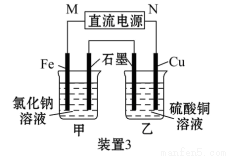
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞试液,观察到石墨电极附近首先变红。
①电源的M端为_________极,甲烧杯中铁电极的电极反应为________________;
②乙烧杯中电解反应的离子方程式为______________;
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,则甲烧杯中产生的气体在标准状况下为________ mL。
查看答案和解析>>
科目:高中化学 来源:2016届山西省忻州市高三上学期第一次月考化学试卷(解析版) 题型:选择题
烃A分子式为C4H10,分子结构中含有一个次甲基(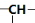 ),则此物质A的二溴代物的种数为
),则此物质A的二溴代物的种数为
A、3种 B、4种 C、5种 D、以上都不对
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期开学考试化学试卷(解析版) 题型:推断题
(10分)下图中A~J均为有机化合物。
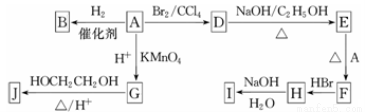
根据图中信息,回答下列问题:
(1)环状化合物A的相对分子质量为82,其中含碳87.80%,含氢12.20%。B的一氯代物仅有一种,B的结构简式为 。
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,则M的结构简式为 。
(3)由A生成D的反应类型是 。
(4)G的分子式为C6H10O4,0.146 g G需用20 mL 0.100 mol·L-1 NaOH溶液完全中和,J是一种高分子化合物。则由G转化为J的化学方程式为 。
(5)分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生如下反应:
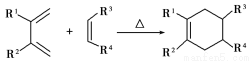 ,
,
则由E和A反应生成F的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期一模化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数,下列叙述正确的是
A.1 mol Cl2在反应中得到电子数不一定为NA
B.1 mol O2在反应中得到电子数一定为4NA
C.1 molNa2O2与足量H2O反应,转移了NA个电子
D.在2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O中,氯气既是氧化产物又是还原产物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省佛山市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.将少量的H2S气体通入硫酸铜溶液中: H2S+Cu2+=CuS↓+2H+
B.将NO2气体通入水中:2NO2+H2O= NO3-+ NO↑+2H+
C.ICl 和Cl2的化学性质相似,将ICl通入KOH溶液中:ICl+2OH-= I-+ ClO-+H2O
D.往100ml 1.5mol/L的FeBr2 溶液中通入0.15mol Cl2:2Br-+Cl2=Br2+2Cl-
查看答案和解析>>
科目:高中化学 来源:2016届贵州省贵阳市高三8月摸底考试化学试卷(解析版) 题型:填空题
(10分)请根据表中数据回答有关问题:
酸或碱 | 电离常数(Ka或Kb) | 难(微)溶物 | 溶度积常数 |
CH3COOH | 1.8×10-5 | BaSO4 | 1×10-10 |
HNO2 | 4.6×10-4 | BaCO3 | 2.6×10-9 |
HCN | 5×10-10 | CaSO4 | 7×10-5 |
HClO | 3×10-8 | ||
NH3·H2O | 1.8×10-5 |
(1)表中所列四种酸中,酸性最弱的是 (用化学式表示)。下列能使醋酸溶液中CH3 COOH的电离度增大,而电离常数不变的操作是 (填序号);
A.升高温度 B.加水稀释
C.加少量的CH3 COONa固体 D.加少量冰醋酸
(2)已知纯水在100℃时的pH=6。该温度下0. lmol/L的NaOH溶液中,pH为 ;
(3)常温下,向水中加入少量醋酸铵固体,所得溶液呈中性,简述其原因 ;
(4)工业中制BaCl2时,需先将BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,欲使SO42-物质的量浓度达到0.01 mol/L以上,则溶液中CO32-物质的量浓度应≥_______mol/L;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com