
| A. | 凡含有食品添加剂的食物对人体健康均有害,不宜食用 | |
| B. | 可用米汤检验含碘盐中的碘酸钾(KIO3) | |
| C. | 涤纶、绵纶、棉花、羊毛、蚕丝等都是天然纤维素 | |
| D. | 纤维素属于糖类,不能够直接被消化成为人体的营养物质 |
分析 A.食品添加剂包括酸度调节剂、抗结剂、消泡剂、抗氧化剂、漂白剂、膨松剂、着色剂、护色剂、酶制剂、增味剂、营养强化剂、防腐剂、甜味剂、增稠剂、香料等;
B.淀粉遇碘单质变蓝色;
C.棉花、羊毛、蚕丝等都是天然纤维素;
D.纤维素属于多糖.
解答 解:A.我国把营养强化剂也归为食品添加剂的范畴,包括对人体有益的某些氨基酸类,盐类,矿物质类,膳食纤维等,故A错误;
B.淀粉遇碘单质变蓝色,碘酸钾不能,故B错误;
C.涤纶、绵纶是合成纤维,故C错误;
D.纤维素属于多糖,人体内无纤维素酶,不能消化纤维素,故D正确.
故选D.
点评 本题考查化学与生活,为高频考点,侧重于基础知识的综合理解和运用的考查,难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
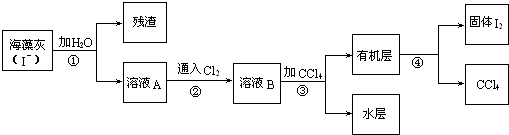
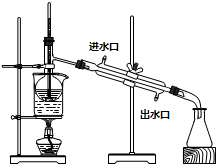
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该晶体中一定含有SCN- | B. | Fe3+的氧化性比I2的氧化性强 | ||
| C. | Fe3+被I-还原 | D. | Fe2+是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M溶液的pH>7 | |
| B. | 25℃时,溶度积常数Ka[NH3•H2O]约为1X10-7 | |
| C. | 25℃时,向M溶液中加少量盐酸,$\frac{c(N{H}_{4}^{+})}{(N{H}_{3}•{H}_{2}O)•c({H}^{+})}$的比值变小 | |
| D. | 25℃时,向1L0.2mol•L-1NH3•H2O溶液中加入1L0.2mol•L-1MgCl溶液,有Mg(OH)2沉淀产生(混合后溶液的体积变化不计) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 恒容通入一定量的SO2 | B. | 增大体系容积 | ||
| C. | 恒容移去部分SO3 | D. | 降低体系温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

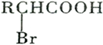
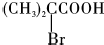 ;
; ,该反应类型为取代反应;
,该反应类型为取代反应;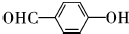 ;
;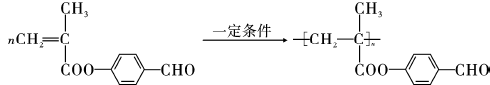 ;
;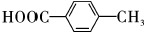 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com