
| A、向水中加入NaHSO4溶液 |
| B、将水加热到100℃,使pH=6 |
| C、向水中加入Al2(SO4)3固体 |
| D、向水中加入CH3COONa固体 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
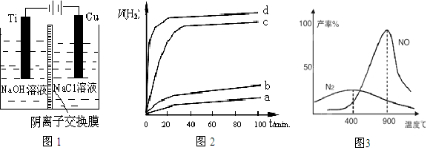
| 方法a | 用炭粉在高温条件下还原CuO | ||||
| 方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O; | ||||
| 方法c | 电解法,反应为2Cu+H2O
| ||||
| 方法d | 用肼(N2H4)还原新制Cu(OH)2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸能与大理石反应产生二氧化碳气体 |
| B、pH=3的醋酸溶液稀释100倍后pH<5 |
| C、室温下,醋酸钠溶液的pH>7 |
| D、常温下,0.1 mol?L-1醋酸溶液pH=2.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、336ml |
| B、224 ml |
| C、448 ml |
| D、112 ml |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3、NaHCO3两种盐的溶液中,离子种类是Na2CO3多于NaHCO3 |
| B、在CH3COONa溶液中c (CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C、在0.1mol?L-1的醋酸溶液中加入适量的蒸馏水,溶液的c(H+)/c(CH3COOH)增大 |
| D、常温下,某溶液中由水电离出的c(H+)为10-5mol/L,则此溶液可能是盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、构成原电池正极和负极的材料必须是两种金属? |
| B、由Cu、Zn作电极与CuSO4溶液组成的原电池中,Cu上产生气泡? |
| C、氢氧燃料电池中,把H2通入正极,此极发生氧化反应 |
| D、在锌铜原电池外电路中,电子由锌流向铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3Cl2+6NaOH=5NaCl+NaClO3+3H2O |
| B、2Br-+Cl2=2Cl-+Br2 |
| C、CaCO3+2HCl=CaCl2+H2O+CO2 |
| D、CO2+Na2O2=Na2CO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4LH2O含有的分子数为1 NA |
| B、32克氧气所含原子数目为4 NA |
| C、1 mol Ca变成Ca2+时失去的电子数为2NA |
| D、1 L 0.1mol?L-1 Na2SO4溶液中有0.1 NA个Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com