
【题目】25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)请写出H2SO3的电离平衡常数K1的表达式:________________。
(2) 常温下,将体积为10mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者_____后者(填“>”、“<”或“=”)。
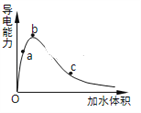
(3)一定条件下,冰醋酸加水稀释过程中溶液导电能力I随加水体积V变化曲线如右图所示,则a、b、c三点溶液醋酸的电离程度由大到小为____________________。
(4)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为___________。
(5)体积相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是_____(填序号)。
(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为________________。
【答案】 ![]() < a<b<c CO32->SO32- >CH3COO->HSO3- ①>②=③ CH3COOH(aq)
< a<b<c CO32->SO32- >CH3COO->HSO3- ①>②=③ CH3COOH(aq) ![]() CH3COO-(aq) + H+(aq) ΔH=+0.3 kJ/mol
CH3COO-(aq) + H+(aq) ΔH=+0.3 kJ/mol
【解析】(1)H2SO3的电离平衡常数K1的表达式:K1=![]() ;(2)CH3COOH的K=1.8×10-5,H2SO3的K1=1.5×10-2,说明亚硫酸强于醋酸,等pH两种酸,醋酸浓度大,当加蒸馏水稀释至1000mL时,醋酸电离出的氢离子多,pH更小些;(3)越稀越电离,则a、b、c三点溶液醋酸的电离程度由大到小为:a<b<c;(4)通过电离平衡常数分析可知,Ka越小,其阴离子越易结合氢离子,则CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为:CO32->SO32- >CH3COO->HSO3-;(5)c(H+)相同的①CH3COOH;②HCl二种酸溶液,酸浓度由大到小的关系是c(CH3COOH) >c(HCl),则体积相同的这两种别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是①>②,而体积相同、c(H+)相同的HCl、H2SO4分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积是相等的,则由大到小的排列顺序是①>②=③;(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,此反应热中包含了H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol和CH3COOH(aq)
;(2)CH3COOH的K=1.8×10-5,H2SO3的K1=1.5×10-2,说明亚硫酸强于醋酸,等pH两种酸,醋酸浓度大,当加蒸馏水稀释至1000mL时,醋酸电离出的氢离子多,pH更小些;(3)越稀越电离,则a、b、c三点溶液醋酸的电离程度由大到小为:a<b<c;(4)通过电离平衡常数分析可知,Ka越小,其阴离子越易结合氢离子,则CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为:CO32->SO32- >CH3COO->HSO3-;(5)c(H+)相同的①CH3COOH;②HCl二种酸溶液,酸浓度由大到小的关系是c(CH3COOH) >c(HCl),则体积相同的这两种别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是①>②,而体积相同、c(H+)相同的HCl、H2SO4分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积是相等的,则由大到小的排列顺序是①>②=③;(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,此反应热中包含了H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol和CH3COOH(aq) ![]() CH3COO-(aq) + H+(aq) ΔH=?,由盖斯定律可求得醋酸电离的反应热,则醋酸电离的热化学方程式为: CH3COOH(aq)
CH3COO-(aq) + H+(aq) ΔH=?,由盖斯定律可求得醋酸电离的反应热,则醋酸电离的热化学方程式为: CH3COOH(aq) ![]() CH3COO-(aq) + H+(aq) ΔH=+0.3 kJ/mol。
CH3COO-(aq) + H+(aq) ΔH=+0.3 kJ/mol。


科目:高中化学 来源: 题型:
【题目】碲(Te)为第五周期元素,与氧同主族,其单质和化合物在化工生产等方面具有广泛应用。
(1)画出碲的原子结构示意图___________________。
(2)已知TeO2微溶于水,易溶于较浓的强酸和强碱。写出TeO2溶于浓氢氧化钠溶液的离子方程式_________________________。
(3)工业上用铜阳极泥(主要成分为Cu2Te,还含有少量的Ag、Au)为原料制备单质碲的工艺流程如下:

①“加压浸出”过程中被氧化的元素为_____________(填元素符号),1molCu2Te被“浸出”时氧化剂得到的电子数为___________________。
②“酸浸”时,温度过高会使碲的浸出率降低,原因为____________________。
③“还原”过程的化学方程式为____________________。
④工业上还可以将铜阳极泥煅烧、碱浸后得到Na2TeO3溶液,然后再通过电解的方法得到单质碲,阴极的电极反应式为______________________ 。
(4)25℃时,向1mol·L-1的Na2TeO3溶液中滴加盐酸,当溶液pH约为6时,此时溶液中c(HTeO3-):c(TeO32-)=_____________。(H2TeO3的Ka1=1.0×10-3,Ka2=2.0×10-8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴、铁、镓、砷的单质及其化合物在生产生活中有重要的应用,请回答下列问题:
(1)写出砷(As)的基态原子的电子排布式_________。
(2)N、P、As为同一主族元素,其电负性从大到小的顺序为_______,它们的简单氢化物沸点最高的是______,将NaNO2和Na2O在一定的条件下反应得到一种白色晶体,已知其中的阴离子与SO42-互为等电子体,则该阴离子的化学式为________。
(3)Fe3+、Co3+、N3+-、CN-等可形成络合离子。
①K3Fe(CN)6]可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为________。
②[Co(N3)(NH3)5]SO4中Co的配位数为_______,其配离子中含有的化学健类型为_____(填离子键、共价键、配位键),C、N、O的第一电离能最大的是_____,其原因是_______。
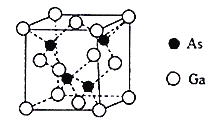
(4)砷化镓晶胞结构如图。晶跑中Ga与周围等距且最近的砷形成的空间构型为_____,已知砷化镓晶胞边长为apm,其密度为ρg·cm-3,则阿伏加德罗常数的数值为______(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度相同的NaOH溶液各100 mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量
的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与
所加盐酸体积之间关系如下图所示。下列判断正确的是
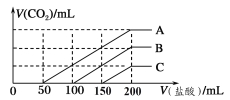
A.通入CO2后,A烧杯中的溶质成分是Na2CO3
B.B烧杯中通入的CO2体积为448 mL
C.原NaOH溶液的浓度为0.2 mol/L
D.通入CO2后,C烧杯中溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL4mol/L的稀硫酸中,生成标准状况下6.72L气体。向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,所得沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系如图所示:
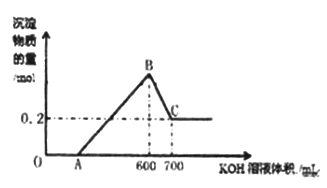
(1)OA对应反应的离子方程式为________________,BC对应反应的离子方程式为_________________;
(2)c(KOH)=_________mol/L,混合物中氧化铝的物质的量为_____mol;
(3)A点对应的数值为_______;
(4)在中学阶段,实验室里检验B点对应的溶液中的阳离子时,所观察到的现象是___________。
(5)向C点对应的溶液中通入足量的CO2所发生反应的离子方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)下图中______(填“A”或“B”)是碱式滴定管,进行该实验的第一步操作是____________________。
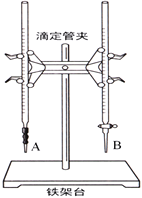
(2)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直到因加入一滴盐酸后,出现_____________________________(填“现象”)说明达到滴定终点。
(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是(____)
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为________mL。
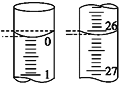
(5)某学生根据3次实验分别记录有关数据如下表:
滴定次数 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | ||
第一次 | 25.00 | 0.00 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 |
第三次 | 25.00 | 0.22 | 26.31 |
依据上表数据列式计算该NaOH溶液的物质的量浓度(写出简要过程)。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素及其化合物在化工、医药、材料等领域有着广泛的应用,回答下列问题:
(1)参照下图B、F元素的位置,依据第二周期元素第一电离能的变化规律,用小黑点标出C、N、O三种元素的相对位置。_________
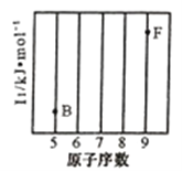
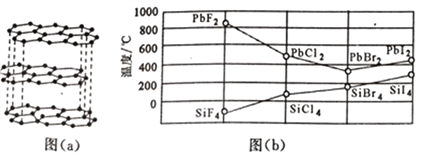
(2)碳的一种单质的结构如图(a)所示,则碳原子的杂化轨道类型为__________________。
(3)二卤化铅PbX2的熔点如图(b)所示,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性__________(填“增强”、“ 不变”或“减弱”,下同),共价性__________。
(4)NH3和F2在Cu催化下可发生反应4NH3+3F2![]() NF3+3NH4F,化学方程式中的5种物质所属的晶体类型有_____(填序号)。写出基态铜原子的价电子排布式_____________。
NF3+3NH4F,化学方程式中的5种物质所属的晶体类型有_____(填序号)。写出基态铜原子的价电子排布式_____________。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
(5)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:
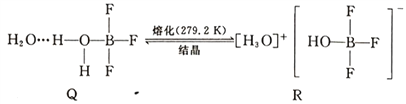
晶体R中含有的化学键包括____________。
(6)水杨酸第一级电离形成离子![]() ,相同温度下,水杨酸的Ka2_________苯酚(
,相同温度下,水杨酸的Ka2_________苯酚(![]() )的Ka(填“>”“ =”或“<”),其原因是_______________。
)的Ka(填“>”“ =”或“<”),其原因是_______________。
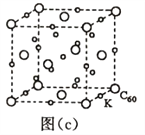
(7)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示,K位于立方体的棱上和立方体的内部,此化合物的化学式为_____________;其晶胞参数为1.4nm,阿伏加德罗常数用NA表示,则晶体的密度为_________g·cm-3。(只需列出式子)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化锶(Sr3N2)在工业上有广泛应用。已知氮化锶遇水剧烈反应产生氢氧化锶和氨气。
锶和镁位于同主族且锶比镁活泼, 锶与氮气在加热条件下反应产生氮化锶。某学习小组拟设计两套方案制备氮化锶:
方案Ⅰ:根据下列装置制备氮化锶。
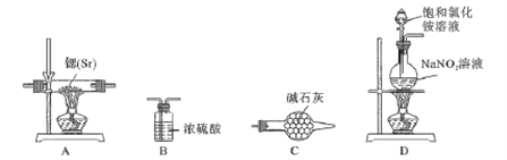
已知:实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气。
回答下列问题:
(1)气流从左至右,选择装置并排序为___________(填字母表示)。
(2)写出实验室制备N2的化学方程式____________
(3)实验时先点燃_____处酒精灯(填“A”或“D”),一段时间后,点燃另一只酒精灯。
(4)氮化锶遇水发生反应的化学方程式为____________
方案Ⅱ:某氮气样品可能含有少量的CO、CO2、O2等气体杂质,某同学设计如下装置制备氮化锶(各装置盛装足量试剂)。已知:醋酸二氨合亚铜CH3COO[Cu(NH3)2]溶液能定量吸收CO,但易被O2氧化,失去吸牧CO能力;连苯三酚鹹性溶液能定量吸收O2.
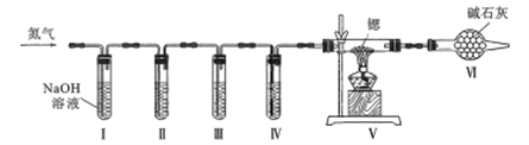
(5)试管Ⅱ盛装的试剂是__________填代号)。
a.连苯三酚碱性溶液b.醋酸二氨合亚铜溶液 C.浓巯酸d.赤热铜粉
装置Ⅵ的作用是_______________
(6)测定产品纯度:取wg产品,向其中加入适量的水。将产生的气体全部通人到依硫酸中,依硫酸增重mg,则产品纯度为__(用代数式表示)。有同学认为上述方法使测得产品纯度偏高,其原因是___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】EPR橡胶(![]() )和PC塑料(
)和PC塑料( )的合成路线如下:
)的合成路线如下:

(1)A的名称是 ___________。
(2)C的结构简式____________。
(3)下列说法正确的是(选填字母)_______________。
A. 反应Ⅱ的原子利用率为100%
B. 反应Ⅲ为取代反应
C. 1 mol E与足量金属 Na 反应,最多可生成标准状况下22.4 L H2
D. CH3OH在合成PC塑料的过程中可以循环利用
(4)反应Ⅰ的化学方程式是_______________________________。
(5)反应Ⅳ的化学方程式是_______________________________。
(6)已知:

以D和乙酸为起始原料合成![]() 无机试剂任选,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明反应试剂和条件)。______________
无机试剂任选,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明反应试剂和条件)。______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com