
����Ŀ�����������Ҫ�ɷ�ΪFeTiO3(�ɱ�ʾΪFeO��TiO2)����������MgO��CaO��SiO2�����ʡ������������Ʊ�����ӵ�ص缫����(�����Li4Ti5O12�����������LiFePO4)�Ĺ�ҵ��������ͼ��ʾ��
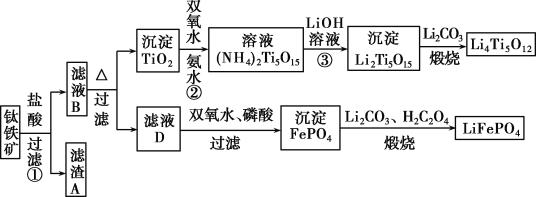
��֪��FeTiO3�����ᷴӦ�����ӷ���ʽΪ��FeTiO3��4H����4Cl��=Fe2����TiOCl![]() ��2H2O��
��2H2O��
��1������ʵ���������չ���������õ����ֹ������ʵ������������������ƾ��ơ��������⣬����________(����������)�������ж���漰��������ϴ�ӳ����ķ����� ��
��2����������������A�Ʊ��뵼��ķ�Ӧ����ʽ��_________________��
��3����ҺB��TiOCl![]() ת������TiO2�����ӷ���ʽ��____________________��
ת������TiO2�����ӷ���ʽ��____________________��
��4����Ӧ���й���TiO2ת����(NH4)2Ti5O15��Һʱ��TiԪ�صĽ������뷴Ӧ�¶��йأ���Ӧ�¶ȹ���ʱ��TiԪ�ؽ����ʻ��½�����ԭ����__________ ____��
��5������ҺD�Ʊ�LiFePO4�Ĺ����У�����˫��ˮ��H2C2O4�����ʵ�������_________��
���𰸡�
��1�����Ǽܡ���������©���м�ˮ����û��������ˮ��Ȼ���º����ظ�2-3�Σ�
��2��2C+ SiO2![]() 2CO + Si��
2CO + Si��
��3��TiOCl42-+H2O=TiO2��+2H++4Cl-��
��4���¶ȹ���ʱ����Ӧ�ﰱˮ(��˫��ˮ)�����ֽ⣻
��5��1��1��
��������
�������������ʯ���������ܽ���˵õ�����Ϊ�������裬��ҺBΪMgCl2��CaCL2��FeCl2��TiCl2�����ȴٽ�ˮ�⣬���˵õ�����TiO2�������������Ͱ�ˮ��Ӧ�õ�(NH4)2Ti5O15���������������Һ�õ�����Li2Ti5O15����̼������յõ������Li4Ti5O12����ҺD����������������������ӣ���������õ�����������������̼��﮺Ͳ������յõ����������LiFePO4��
��1���ڿ��������չ�������Dʱ�����õ��������������������ǡ����Ǽܡ��ƾ��ƣ���������������ϴ�ӷ�������©���м�ˮ����û��������ˮ��Ȼ���º����ظ�2-3�Σ��ʴ�Ϊ�����Ǽܡ���������©���м�ˮ����û��������ˮ��Ȼ���º����ظ�2-3�Σ�
��2�����������ж������費�������ᣬ��������A�ɷ��Ƕ������裬����������̼�ڸ����·�Ӧ���ɹ��һ����̼����Ӧ����ʽΪ2C+ SiO2![]() 2CO + Si���ʴ�Ϊ��2C+ SiO2
2CO + Si���ʴ�Ϊ��2C+ SiO2![]() 2CO + Si��
2CO + Si��
��3���������̿�֪��TiOCl42-����Һ�м�����ˮ��Ӧ���ɶ������ѳ�������Ӧ�����ӷ���ʽΪ��TiOCl42-+H2O=TiO2��+2H++4Cl-���ʴ�Ϊ��TiOCl42-+H2O=TiO2��+2H++4Cl-��
��4�����ڶ��������백ˮ��˫��ˮ��Ӧ����(NH4)2Ti5O15ʱ���¶ȹ��ߣ�˫��ˮ�Ͱ�ˮ�����ֽ⣬���Է�Ӧ�¶ȹ���ʱ��TiԪ�ؽ������½����ʴ�Ϊ���¶ȹ���ʱ����Ӧ�ﰱˮ(��˫��ˮ)�����ֽ⣻
��5�����ݵ����غ㣬������Ԫ��ת�Ƶĵ��Ӿ͵�����������������ת�Ƶĵ���������˿ɵù�ϵʽ��H2O2��H2C2O4��˫��ˮ��H2C2O4�����ʵ�����Ϊ1��1���ʴ�Ϊ��1��1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������Һ��Ӧ����
A. ������ B. ��֬ C. �Ҵ� D. ��ά��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z��ԭ��������������W�ĵ�����H2�ڰ����ܻ��ϲ�������ը��X��ͬ�����н�������ǿ��Ԫ�أ�Yԭ�ӵ��������������ڵ��Ӳ�����W��Zԭ�ӵ�������������ͬ������˵��������ǣ� ��
A. ���ʵķе㣺Z��W
B. �����Ӱ뾶��X��W
C. Ԫ��X�������γɼȺ����Ӽ�Ҳ���Ǽ��Թ��ۼ��Ļ�����
D. X��Y��Z������������Ӧ��ˮ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������и�ͼ���˵������ȷ����
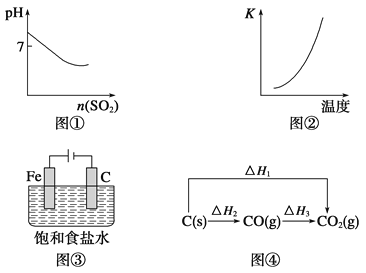
A��ͼ����ʾ��SO2����ͨ����ˮ��
B��ͼ����ʾ��ӦN2(g)��3H2(g) ![]() 2NH3(g) ��H��0��ƽ�ⳣ��K���¶ȵı仯
2NH3(g) ��H��0��ƽ�ⳣ��K���¶ȵı仯
C��ͼ���������������ռ������������֮��һ��Ϊ1��1
D��ͼ���еĦ�H1����H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��100mL 1molL��1Al2��SO4��3��Һ�У���Al3+���ӵ����ʵ����� ��
A.0.1mol
B.0.2mol
C.0.3mol
D.0.4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����xR2+ +yH++O2��mR3+ +nH2O�����ӷ���ʽ�У���m��R3+�ж���ȷ���ǣ�
A. m��4��R3+����������
B. m��2y��R3+����������
C. m��2��R3+�ǻ�ԭ����
D. m��y��R3+�ǻ�ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����ʽ�ɼ���������Ԫ�ؼ��仯��������ʡ���֪
������ԭ��Ӧ��
2FeCl3��2HI=2FeCl2��I2��2HCl��
2Co(OH)3��6HCl=2CoCl2��Cl2����6H2O��
2Fe(OH)2��I2��2KOH=2Fe(OH)3��2KI��
3I2��6KOH=5KI��KIO3��3H2O
���ֽⷴӦ��
2HSCN��K2CO3=2KSCN��CO2����H2O��
KCN��CO2��H2O=HCN��KHCO3
�ȷֽⷴӦ��
4NaClO![]() 3NaCl��NaClO4��NaClO4
3NaCl��NaClO4��NaClO4![]() NaCl��2O2��
NaCl��2O2��
����˵������ȷ����
A�����ȶ��ԣ�NaCl��NaClO4��NaClO
B����ԭ��(������Һ)��Fe(OH)2��I2��KIO3
C��������(������Һ)��FeCl3��Co(OH)3��I2
D������(ˮ��Һ)��HSCN��H2CO3��HCN
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������һ�ֽ�������������(������ˮ�������������)����Һ������Һ���������ӵ�Ũ�Ⱦ�������ܴﵽ��Ŀ�ĵ���(����)
A. Na+��Mg2+��SO42����Cl- B. ClO-��I-��NH4����Ba2+
C. Na+��AlO2����K+��HCO3�� D. Al3+��K+��SO42����NO3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com