已知:A、B、C、D、E、F、G七种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,原子序数依次增大,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,A与F、E与F组成的化合物是机动车排出的大气污染物,G是原子半径最小的元素.试推断回答下列问题:
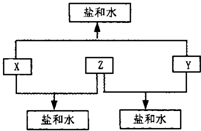
(1)D元素周期表中的位置为
A、B、C三种元素的离子半径由小到大的顺序为
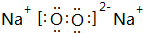
(用元素符号表示).由以上元素中两两形成的化合物中,含有离子键和非极性共价键的化合物的电子式为
.
(2)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式
; A的气态氢化物2.24L(标准状况)被 200mL 1moL/L X溶液吸收后,所得溶液中离子浓度从大到小的顺序是
.
(3)一定温度下,向2L密闭容器中充入2molA
2和4molG
2,若保持体积不变,0.5min后达到平衡,测得容器中有1mol AG
n,则平均反应速率v(A
2)=
.若保持温度和体积不变,向平衡体系中加入 1mol G
2和1molAG
n,则平衡的移动方向
(填“正反应方向”、“逆反应方向”或“不移动”﹚.


 ,
, ;
;

 (2011?新余二模)化学--选修物质结构与性质
(2011?新余二模)化学--选修物质结构与性质
 已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.

 已知单质A、B、C、D有如下的反应关系.其中A 在B中燃烧时,火焰呈苍白色; C在B中燃烧时生成棕黄色的烟,E的水溶液呈蓝绿色,G是一种黑色固体.
已知单质A、B、C、D有如下的反应关系.其中A 在B中燃烧时,火焰呈苍白色; C在B中燃烧时生成棕黄色的烟,E的水溶液呈蓝绿色,G是一种黑色固体.