
【题目】为了除去氧化铁粉中混有的少量铝粉所选试剂和操作都合理的是
A.盐酸,蒸发B.盐酸,过滤
C.NaOH溶液,蒸发D.NaOH溶液,过滤
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】ZnCI2是重要的工业原料,在电化学、冶金、印染等领域用途广泛,以某厂排放的废酸液(主要成分为盐酸,含Fe2+、Cu2+、Ni2+、H3AsO3等杂质)和锌蓄电池废渣(主要成分为ZnO、Zn)为原料制备ZnCl2的流程如图所示:

已知:
①25℃时,Ksp[Fe(OH)3]=4.0×10-38;Ksp[Zn(OH)2]=1.2×10-17;Ksp[Ni(OH)2]=2.0×10-15;
②溶液中的离子浓度小于等于10-5 mol·L-1时,认为该离子沉淀完全。
请问答下列问题:
(1)在元素周期表中,砷(As)元索与氮元素同主族且处于第4 周期,则砷元素的最简单氢化物的电子式为_______________;其最高价氧化物对应水化物的化学式为___________________。
(2)“浸出”过程中主要生成两种单质,其化学式为________________。
(3)控制温度为75℃左右,向滤液1中加人H2O2,生成FeAsO4的离子方程式为_________。此过程中,所加入H2O2的量需适当大于理论值,原因因为____________。
(4)蒸发滤液3制备ZnCl2时,需不断通人HC1的理由为____________。
(5)某纽扣电池放电时,总反应为Zn+Ag2O+H2O═Zn(OH)2 + 2Ag,其正极反应式为______________。
(6)25℃时,向浓度为1.0 mol·L-1的Fe3+、Zn2+、Ni2+的混合溶液中滴加NaOH溶液,当Fe3+恰好沉淀完全时,所得溶液中c(Zn2+):c(Ni2+)=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列说法中正确的是( )
A. 标准状况下,2.24LCHC13含有的分子数为0.1NA
B. 0.1molCnH2n+2中含有的碳碳单键数为0.1nNA
C. 2.8g乙烯和丙烯的混合气体中所含碳原子为0.2NA
D. 1mol苯乙烯中含有的碳碳双键数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作所用仪器合理的是 ( )
A. 用广泛pH试纸测得Na2CO3溶液的pH为10.5
B. 用10mL量筒量取5.20mL盐酸
C. 用托盘天平称取25.20gNaCl
D. 用25mL的酸式滴定管量取14.80mL KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 铜的金属活泼性比铁的弱,可在海轮外壳上镶入若干铜块以减缓其腐蚀
B. 若反应过程中断开化学键放出的能量大于形成化学键所吸收的能量,则反应放热
C. 一定温度下,增大反应2BaO2(s)![]() 2BaO(s)+O2(g)容器的体积,平衡不移动
2BaO(s)+O2(g)容器的体积,平衡不移动
D. 反应CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH>0能自发进行,可知该反应ΔS>0
CO(g)+H2O(g) ΔH>0能自发进行,可知该反应ΔS>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3是一种重要的化工原料,可以制备一系列物质(见图)。下列说法正确的是
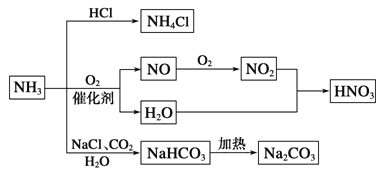
A. NH4Cl和NaHCO3都是常用的化肥
B. NH4Cl、HNO3和Na2CO3受热时都易分解
C. NH3和NO2在一定条件下可发生氧化还原反应
D. 图中所涉及的反应均为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al(NO3)3 常用于![]() 的萃取。测量Al(NO3)3 纯度的实验步骤如下图所示。下列说法正确的是( )
的萃取。测量Al(NO3)3 纯度的实验步骤如下图所示。下列说法正确的是( )

A. 配置Al(NO3)3 溶液需要的玻璃仪器只有250 mL容量瓶,玻璃棒
B. 加入试剂a发生反应的离子方程式为Al3++3OH—=Al(OH)3↓
C. 操作“b ”需要在蒸发皿中进行
D. Al(OH)3的纯度为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的俗名与化学式对应正确的是( )
A. 食盐——NaCl B. 铁红——Fe3O4
C. 明矾——Al2(SO4)3 D. 烧碱——Ca(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com