
对于任何一个化学平衡体系,以下变化或采取的措施,使平衡一定发生移动的是:
①加入一种反应物 ②增大体系的压强 ③升高温度 ④使用催化剂 ⑤化学平衡常数减小
A.①②③⑤ B.①②③④⑤ C.③⑤ D.①②③
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
Ⅰ (本题4分)赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合物加热有以下反应发生:2Cu2O+Cu2S 6Cu+SO2↑ 填写下列空白:
6Cu+SO2↑ 填写下列空白:
①在该反应中,氧化剂是 。还原剂是 。
②氧化产物与还原产物的质量比是 。
Ⅱ(本题7分)A、B、C、D、E为易溶化合物,其离子组成为
| 阳离子 | Fe3+、Ba2+、Al3+、Na+、Ag+ |
| 阴离子 | NO3—、OH—、SO42—、Cl—、CO32— |
在各化合物中离子不重复,分别取其溶液进行实验,结果如下:
①在A溶液中逐滴加入氨水,有白色沉淀生成,继续加氨水至过量,沉淀消失;
②用pH试纸测得B和C溶液显碱性,0.1mol/L的C溶液pH小于13;
③在D溶液中加入铁粉,溶液质量增加且无气体产生;
④在E溶液中加入过量B,没有沉淀产生。
完成下列填空:
(1)A的化学式为 ;
(2)③反应的离子方程式为 ;
(3)检验D溶液中阴离子的的方法是 ;
(4)E的的化学式为 ,将E蒸干、灼热至质量不再改变,最后所得物质是(填化学式) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某恒温密闭容器发生可逆反应Z(?)+W(?) X(g)+Y(?) ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积, t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是:
X(g)+Y(?) ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积, t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是:
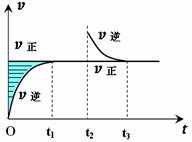 A.Z和W在该条件下一定不为气态
A.Z和W在该条件下一定不为气态
B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
C.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度相等
D.若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是

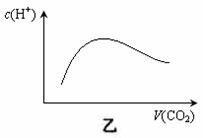
A.由甲可知,A与B在有催化剂存在的热化学方程式为: 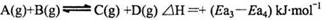
B.常温常压下,将a mol CO2气体通入1L bmol/L的NaOH溶液中,当a=2b时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如图乙变化关系;当1/2<a/b<1时,所得溶液中一定存在: c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
C.常温下,将稀NaOH溶液与CH3COOH溶液混合,不可能出现pH>7,
且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)的情况
D.某温度下,pH=11的NH3·H2O和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3·H2O与NH3三种微粒的平衡浓度之和为0.05mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
常温时,向pH=2的硫酸溶液中加入等体积的下列溶液后,滴入甲基橙试液出现红色,该溶液可能是
①pH=12的Ba(OH)2 ②pH=12的氨水
③0.005mol·L-1NaOH ④0.05mol·L-1BaCl2
A.①② B.②③ C.③④ D.④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com