
下列各指定微粒的数目比不是1∶1的是
A.Na2O2中阴离子和阳离子 B.NaOH晶体中阳离子和阴离子
C. Mg2+离子中的质子和中子 D.氯化钠中的质子总数和电子总数
Mg2+离子中的质子和中子 D.氯化钠中的质子总数和电子总数
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
已知25 ℃时有关弱酸的电离平衡常数:( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡 常数(25 ℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
则下列有关说法正确的是
A.等物质的量浓度的各溶液pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.amol·L—1HCN溶液与amol·L—1NaOH溶液等体积混合后,所得溶液显碱性(pH>7),则c (OH-)>c(H+),c(Na+)>c(CN-)
C.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-) +c(CO )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数的值,下列说法正确的是
A.在高温高压下,28 gN2和6g H2充分反应生成NH3的分子数为2NA
B.1mol/LFeCl3 溶液中所含Fe3+的数目小于NA
C.常温下,1L pH=12的Ba(OH)2 溶液中含OH—的数目为2NA
D.23g NO2和N2O4的混合气体中含有氮原子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
“神七”登天标志着我国的航天事业进入了新的篇章。
(1)火箭升空需要高能的燃料,经常是用四氧化二氮和联氨(N2H4)作为燃料,工业上利用氮气和氢气可以合成氨气,氨又可以进一步制备联氨等。
已知 N2(g)+2O2(g)=2NO2(g) △H =+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =— 534.0kJ/mol
NO2(g)  1/2N2O4(g) △H = —26.35kJ/mol
1/2N2O4(g) △H = —26.35kJ/mol
①写出气态联氨在气态四氧化二氮中燃烧生成氮气和水蒸气的热化学方程式 ▲ ;
②用氨和次氯酸钠按一定物质的量之比混合反应可生成联氨,该反应的化学方程式为 ▲ ;
(2)下图是某空间站能量转化系统的局部示意图,其中燃料电池采用氢氧化钾为电解液,燃料电池放电时的负极反应式为 ▲ ,
如果某段时间内氢氧储罐中共收集到33.6 L气体(已折算成标准状况),则该段时间内水电解系统中转移电子的物质的量为 ▲ mol。
 |
(3)在载人航天器的生态系统中,不仅要求分离除去CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2 = 2CO + O2,CO可用作燃料。
已知该反应的阳极反应为:4OH--4e-= O2↑ + 2H2O,则阴极反应式为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ、一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
 (1)此反应的化学方程式中
(1)此反应的化学方程式中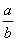 =__________
=__________
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:
(3)平衡时,N的转化率为 。
(4)下列叙述中能说明上述反应达到平衡状态的是
A.反应中M与N的物质的量之比为1︰1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
F.N的质量分数在混合气体中保持不变
II、某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:
实验①:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示:

实验②:把纯锌片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气的量减少。
实验③:在盐酸中滴入几滴CuCl2溶液,生成氢气速率加快。
试回答下列问题:
(1)试分析实验①中t1~t2速率变化的主要原因是 ,t2~t3速率变化的主要原因是 。
(2)实验②放出氢气的量减少的原因是 。
(3)某同学认为实验③反应速率加快的主要原因是因为形成了原电池,你认为是否正确?
(填“正确”或“不正确”)。请选择下列相应的a或b作答。
a、若不正确,请说明原因:
b、若正确则写出实验③中原电池的正极电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法正确的是 ( )。
A.常温下,4 g CH4含有NA个C—H共价键
B.1 mol Fe 与足量的稀HNO3反应,转移2NA个电子
C.1 L 0.1 mol·L-1 NaHCO3溶液中含有0.1NA 个HCO3-
D.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列叙述正确的是 ( )。
A.25 ℃,1 L pH=1的稀硫酸中含有的H+数为0.1 NA
B.标准状况下,224 mL水含有的电子数为0.1 NA
C.常温常压下,0.56 L甲烷中含有的共价健数为0.1 NA
NA
D.0.15 mol NO2与水完全反应时转移的电子数为0.15 mol NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )。
A.氯化钠在电流的作用下电离出Na+和Cl-
B.CaCO3难溶于水,但CaCO3属于强电解质
C.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
D.硫酸钠在水中的电离方程式可表示为Na2SO4===2Na++S6++4O2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com