
【题目】H2O2既可以作氧化剂,又可以作还原剂。现在H2O2溶液中加入用硫酸酸化的KMnO4溶液,紫红色的KMnO4溶液变成了无色溶液。该反应体系中共七种物质:O2、KMnO4、MnSO4、H2SO4、K2SO4、H2O、H2O2。
(1)请将以上反应物与生成物分别填入以下空格内___。
![]()
(2)该反应中的还原剂是__(填化学式)被还原的元素是____(填元素符号)。
(3)如反应中电子转移了0.5mol,则产生的气体在标准状况下的体积为__L。
(4)+6价铬的化合物毒性较大,酸性溶液中常用NaHSO3将废液中的Cr2O72-还原成Cr3+,该反应的离子方程式为___。
【答案】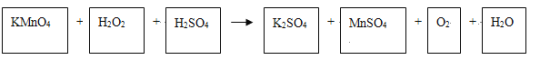 H2O2 Mn 5.6L 3HSO3-+ Cr2O72- +5H+= 2Cr3++3SO42-+4H2O
H2O2 Mn 5.6L 3HSO3-+ Cr2O72- +5H+= 2Cr3++3SO42-+4H2O
【解析】
H2O2溶液中加入用硫酸酸化的KMnO4溶液,紫红色的MnO4-被还原成了无色Mn2+,则反应中H2O2应被氧化,生成氧气和水,结合氧化剂和还原剂之间得失电子数目相等配平化学方程式,则反应物和生成物的转化关系为2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O;反应中MnO4-被还原,Mn元素化合价降低,H2O2被氧化,H2O2为还原剂;根据转移的电子的物质的量与生成物氧气之间的关系计算产生的气体在标准状况下的体积;根据元素守恒,电荷守恒,写出化学方程式,并且配平。
(1)H2O2溶液中加入用硫酸酸化的KMnO4溶液,紫红色的MnO4-被还原成了无色Mn2+,则反应中H2O2的化合价升高,应被氧化,生成氧气和水,KMnO4+H2O2+H2SO4→K2SO4+MnSO4+O2↑+H2O 结合氧化剂和还原剂之间得失电子数目相等配平化学方程式,则反应物和生成物的转化关系为2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O;
(2)反应中MnO4-中的Mn元素化合价降低,是被还原的元素,H2O2被氧化,H2O2为还原剂;
(3)根据反应方程式2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O可知,Mn元素化合价从+7降低到+2价,有2个锰原子化合价降低,2molKMnO4参加反应共转移了10mol电子,过氧化氢中氧原子的化合价从-1价升高到0价,剩余的四个氧原子从-2价升高到0价,共转移10mol电子,产生气体的物质的量为5mol,则反应中电子转移了0.5mol,则产生的气体的物质的量为0.25mol,在标准状况下的体积为0.25mol ×22.4L/mol=5.6L;
(4)+6价铬的化合物毒性较大,酸性溶液中常用NaHSO3将废液中的Cr2O72-还原成Cr3+,氧化还原反应中有元素的化合价升高,就有元素的化合价降低,Cr元素化合价由+6价降低为+3价,则NaHSO3中S元素的化合价应该有+4价升高为+6价,根据元素守恒,电荷守恒,该反应的离子方程式为3HSO3-+ Cr2O72- +5H+=2Cr3++3SO42-+4H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果不正确的是( )

A.图中,AB段的反应为Fe+2Fe3+=3Fe2+,溶液中溶质最终为硫酸亚铁
B.原溶液中硫酸浓度为2.5 mol·L-1
C.原混合溶液中硝酸根离子的物质的量为0.2 mol
D.图中,OA段产生的气体是一氧化氮,BC段产生的气体是氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化一定属于化学变化的是( )
①金属导电 ②燃烧 ③煤的干馏 ④焰色反应 ⑤无水硫酸铜吸水 ⑥工业制氧气 ⑦白磷转变成红磷 ⑧久置浓硝酸变黄 ⑨丁达尔现象 ⑩煤旳液化
A.①④⑨B.⑥⑧⑩C.②⑥⑦D.②③⑤⑦⑧⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中离子在水溶液中能大量共存且满足相应要求的是( )
选项 | 离子 | 要求 |
A | K+、NO | c(K+)<c(Cl-) |
B | Na+、NO | 逐滴滴加盐酸立即有气体产生 |
C | Na+、Al3+、Mg2+、SO | 逐滴滴加氨水立即有沉淀产生 |
D | NH | 滴加NaOH浓溶液立刻有气体产生 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】历史上金、银、铜主要是作为货币金属或装饰品被应用。
(1)金、银、铜常被作为钱币流通,从化学角度来看,主要是利用它们的________(填字母)。
A.硬度适中
B.密度适中
C.在自然界里都可得到纯净的单质
D.不活泼性
(2)提炼黄金的过程一般要使用化学药品氰化物,其直接后果是________(填字母)。
①污染水体 ②破坏臭氧层 ③危害工人的生命与健康 ④破坏植被
A.①② B.①②③
C.②④ D.①③④
(3)古代的“药金”外观与金相似,常被误认为金子。它的冶炼方法如下:将ZnCO3、赤铜(Cu2O)、木炭混合加热到800 ℃,得到金光闪闪的“药金”,则药金的主要成分是________,有关化学方程式为__________________________
(4)用“药金”制成的假金元宝欺骗人的事件屡有发生。下列能区别其真伪的方法是________(填字母)。
A.测定密度 B.放入硝酸中
C.放入盐酸中 D.观察外表
(5)在化学反应中,铜元素可表现为0、+1、+2价。在西汉古籍中曾有记载:曾青得铁则化为铜[即:曾青(CuSO4)跟铁反应就生成铜]。试写出该反应的化学方程式:_____________。
(6)铜器表面有时会生成铜绿[Cu2(OH)2CO3],这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物反应的化学方程式:__________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种利用H2C2O4(草酸)作助溶剂,酸浸提取硫酸烧渣(主要含Fe2O3、FeO、SiO2等)制备铁红并回收副产物硫酸铵的工艺流程如图:
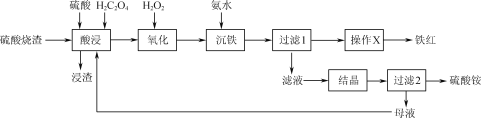
已知:H2C2O4可沉淀Ca2+、Fe2+等金属离子,可与Fe3+生成[Fe(C2O4)3]3-,在硫酸作用下可热分解生成CO和CO2。
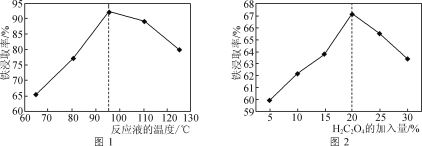
(1)用50%的硫酸“酸浸”时,反应液的温度、H2C2O4的加入量对铁浸取率的影响分别如图1、图2所示:
①“硫酸烧渣”中Fe2O3与H2SO4反应的化学方程式为___。
②图1中,反应液的温度高于95℃时,铁浸取率开始降低,其原因是___。
③图2中,H2C2O4加入量在5~20%时,铁浸取率随加入量的增大而增大,其原因是__;H2C2O4加入量超过20%时,铁浸取率反而开始降低,其原因是___。
(2)“沉铁”时发生的主要反应的离子方程式为____。
(3)由“过滤1”的滤渣制备铁红的“操作X”为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,对于可逆反应A(g)+2B(g)![]() 3C(g)的下列叙述中,能说明反应已达到平衡的是
3C(g)的下列叙述中,能说明反应已达到平衡的是
A.单位时间内消耗a mol A,同时生成3a mol CB.容器内的压强不再变化
C.![]() D.C的体积分数不再变化
D.C的体积分数不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2广泛用于水处理、纸浆漂白等。
(1)制备ClO2原料有NaClO2等,产生的ClO2(g)用蒸馏水吸收得到吸收液A。
①ClO2中氯元素的化合价为___。
②NaClO2与盐酸在微热条件下生成ClO2气体(及少量副产物Cl2),写出其反应生成ClO2、NaCl和水的化学方程式:___。
(2)碘量法测定ClO2吸收液A中ClO2和Cl2的浓度的主要实验步骤如下:
步骤1.向锥形瓶中加入50mL蒸馏水、25mL100g·L-1KI溶液(足量),再向其中加入5.00mLClO2吸收液(发生反应:2ClO2+2KI=2KClO2+I2,Cl2+2KI=2KCl+I2)。
步骤2.用0.1000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉溶液,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液6.00mL。
步骤3.向步骤2的溶液中加入5mL2mol·L-1硫酸溶液酸化,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O。
步骤4.重复步骤2操作,第二次滴定又消耗0.1000mol·L-1Na2S2O3溶液20.00mL。
根据上述数据,计算ClO2吸收液A中ClO2和Cl2的浓度___(单位g·L-1,写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中的∣△H∣能表示可燃物的燃烧热的是( )
A.H2(g)+![]() O2(g)=H2O(1)△H=-285.8kJ/mol-1
O2(g)=H2O(1)△H=-285.8kJ/mol-1
B.H2(g)+C12(g)=2HCl(g)△H=-184.6kJ/mol-1
C.2CO(g)+O2(g)=2CO2(g)△H= 一566kJ/mol-1
D.CH4(g)+2O2(g)=2H2O(g)+CO2(g)△H= 一802.3kJ/mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com