

A.电解水制氢:2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
B.高温使水分解制氢:2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
C.太阳光催化分解水制氢:2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
D.天然气制氢:CH4+H2O CO+3H2 CO+3H2 |
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
 2SO3,已知V(SO2)==0.05mol·l-1·min-1,则2min后SO3的浓度为( )
2SO3,已知V(SO2)==0.05mol·l-1·min-1,则2min后SO3的浓度为( )| A.1mol·l-1 | B.0.1mol·l-1 | C.0.9mol·l-1 | D.0.2mol·l-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO(g)+3H2(g);△H=+206.lkJ·mol-l。
CO(g)+3H2(g);△H=+206.lkJ·mol-l。
| A.v(正)>v(逆) | B.v(正)<v(逆) |
| C.v(正)=v(逆) | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.明矾净水的原理是Al3+水解产生Al(OH)3胶体,Al(OH)3胶体能吸附水中的悬浮杂质,并使之沉降 |
| B.摩尔盐的制备原理为:6H2O+FeSO4+(NH4)2SO4=(NH4)2Fe(SO4)?6H2O,反应之所以能进行的原因是(NH4)2Fe(SO4)?6H2O溶解度最小 |
| C.镀锌铁皮在酸中溶解,当镀层反应完全时,产生氢气的速率会突然减慢 |
| D.将火柴头直接浸入品红溶液中,可以检验火柴头中是否含有硫元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示: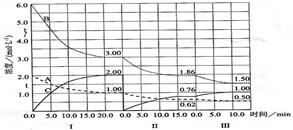
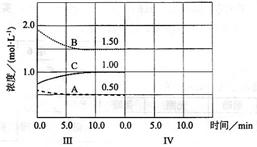
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g) ΔH=-92.20 kJ·mol-1。
2NH3(g) ΔH=-92.20 kJ·mol-1。| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | N2 | 1.00 | 1.00 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量.
是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量.查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pC(g)+qD(g);ΔH<0。下列结论中正确的是( )
pC(g)+qD(g);ΔH<0。下列结论中正确的是( ) 增大1倍,此时A的浓度变为原来的0.48 倍,则m+n>p+q
增大1倍,此时A的浓度变为原来的0.48 倍,则m+n>p+q 平衡时,A.B的转化率相等,说明反应开始A.B的物质的量之比为m∶n
平衡时,A.B的转化率相等,说明反应开始A.B的物质的量之比为m∶n查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com