
(1)氯酸是一种强酸,氯酸的浓度超过40%就会迅速分解,反应的化学方程式为:8HClO3=3O2↑+2Cl2↑+4HClO4+2H2O。 根据题意完成下列小题:
根据题意完成下列小题:
①在上述变化过程中,发生还原反应的过程是______________→______________(填化学式)。
②该反应的氧化产物是____________(填化学式);求所得混合气体的平均相对分子质量。
(2)已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn 2+、H2O、IO
2+、H2O、IO 、MnO
、MnO 、IO
、IO 。
。
①有关反应的离子方程式为__________________。
②在锰离子转化为高锰酸根离子的反应中,如果把反应后的溶液稀释到1 L,测得溶液的pH=2,求在反应中转移电子的物质的量 mol。
科目:高中化学 来源:2016-2017学年河南省南阳市高二上第二次月考化学卷(解析版) 题型:选择题
下列说法中正确的是( )

A.Na2S2O3+2HCl==2NaCl+S↓+SO2↑+H2O在加热条件下化学反应速率增大的主要原因是该反应是吸热反应,加热使平衡向正反应方向移动
B.若在恒容容器中发生反应:N2+3H2 2NH3,达到平衡后再充入适量He,由于压强增大,化学平衡向正反应方向移动
2NH3,达到平衡后再充入适量He,由于压强增大,化学平衡向正反应方向移动
C.在合成氨反应中,其他条件相同时,在有催化剂时(a)和无催化剂时(b)的速率—时间图像可用图一表示
D.若在恒压容器中发生反应:2SO3 2SO2+O2,达到平衡后再充入适量He,其速率—时间图像可用图二表示
2SO2+O2,达到平衡后再充入适量He,其速率—时间图像可用图二表示
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高二上第二次月考化学卷(解析版) 题型:选择题
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是( )

A.a为CH4,b为CO2
B.CO32-向负极移动
C.此电池在常温时也能工作
D.正极电极反应式为O2+2H2O+4e-=== 4OH-
查看答案和解析>>
科目:高中化学 来源:2017届西藏日喀则区第一高级中学高三上期中化学试卷(解析版) 题型:选择题
下列关于各图的说法,正确的是 ( )
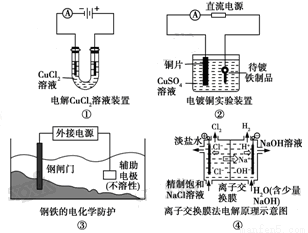
A.①中阴极处能产生使湿润淀粉?KI试纸变蓝的气体
B.②中待镀铁制品应与电源正极相连
C.③中钢闸门应与外接电源的正极相连
D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三10月检测化学试卷(解析版) 题型:填空题
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下:

回答下列问题:
(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
① ZnFe2O4中Fe的化合价是___________,从物质分类角度说,ZnFe2O4属于__________(填“酸”、“碱”或“盐”)。
② 工业上利用反应ZnFe2(C2O4)3·6H2O ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是______________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是______________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。
(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率。为达到这一目的,还可采用的措施是___________(任答一条);已知ZnFe2O4能溶于酸,则酸浸后溶液中存在的金属离子有______________。
(3)净化Ⅰ中H2O2参与反应的离子方程式为_______________;试剂X的作用是___________。
(4)钢铁镀锌是钢铁防护的一种有效方法。按图甲装置进行模拟铁上镀锌的实验,实验结果如图乙所示。乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量。
① C电极的电极反应式为________________________。
② E可以表示的量是_________________________(任写一种)。

查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三10月检测化学试卷(解析版) 题型:选择题
下列各种操作中.不会导致液体分散系颜色发生两次显著变化的是( )
A.向Fe(OH)3胶体中加入4 mol/LH2SO4至过量
B.向紫色石蕊试剂中通入过量Cl2
C.向紫色石蕊试剂中通入过量SO2
D.向酚酞试液中加入Na2O2粉末至过量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com