
| A. | 0.5mol Na完全被氧化生成Na2O2时,转移电子的数目为0.5NA | |
| B. | 0.1molO3中所含氧原子数目为0.2NA | |
| C. | 0.1mol•L-1的NaF溶液中所含F-的数目小于0.1NA | |
| D. | 标准状况下,2.24L CCl4中含有的C-Cl数目为0.4NA |
分析 A.钠生成过氧化钠,化合价由0价升高到+1价;
B.1个臭氧分子中含有3个氧原子;
C.溶液体积未知;
D.气体摩尔体积适用对象为气体.
解答 解:A.0.5 mol Na变为0.25molNa2O2,转移电子数为0.5NA,故A正确;
B.1个臭氧分子中含有3个氧原子,0.1molO3中所含氧原子数目为0.3NA,故B错误;
C.溶液体积未知,无法计算氟离子个数,故C错误;
D.标准状况下,四氯化碳为液体,不能使用气体摩尔体积,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的有关计算,明确有关物质的量的计算公式是解题关键,注意气体摩尔体积只适用于气体,不适用于固体和液体,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 除去保温瓶中的水垢 | B. | 检验自来水中是否含有Cl- | ||
| C. | 检验买来的奶粉中是否加有淀粉 | D. | 洗去白色衣服上的番茄汁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 操作 | |
| A | 比较水和乙醇中羟基氢的活泼性 | 用金属钠分别与水和乙醇反应 |
| B | 证明HOCH2CHO中含有醛基 | 滴加酸性KMnO4溶液,看紫红色是否褪去 |
| C | 确定磷、砷两元素非金属性的强弱 | 测定同温同浓度的Na3PO4和Na3AsO4水溶液的pH |
| D | 除去苯中混有的苯酚 | 向混合液中加入NaOH溶液,充分反应后,分液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| B | 其他条件不变,压缩2HI(g)?I2(g)+H2(g)平衡体系的体积 | 混合气体颜色变深 | 平衡向生成I2(g)的方向移动 |
| C | 将碱式滴定管下部的胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠 | 使溶液从尖嘴流出 | 排出碱式滴定管尖嘴部分的气泡 |
| D | 向2.0mL浓度均为0.1mol•L-1的KCl、KI混合溶液中滴加1-2滴0.01mol•L-1AgNO3溶液,振荡 | 沉淀呈黄色 | KSP(AgCl)>KSP(AgI) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
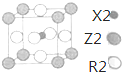 X、Y、Z、W、R是原子序数依次增大的前四周期元素(稀有气体除外).X的基态原子中的电子平均分布在三个不同的能级中;Y的族序数是其周期数的三倍;Z的基态原子核外无未成对电子;W为前四周期中电负性最小的元素;元素R位于周期表的第10列.
X、Y、Z、W、R是原子序数依次增大的前四周期元素(稀有气体除外).X的基态原子中的电子平均分布在三个不同的能级中;Y的族序数是其周期数的三倍;Z的基态原子核外无未成对电子;W为前四周期中电负性最小的元素;元素R位于周期表的第10列.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
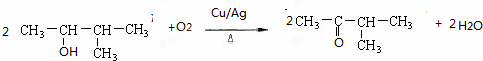 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
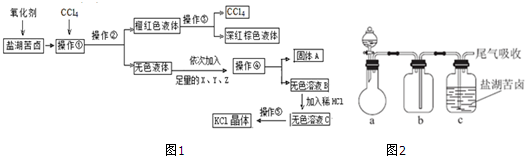
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z、W的原子半径依次减小 | |
| B. | W与X形成的化合物中只可能含有离子键 | |
| C. | 在工业上X、Y都可以直接用加热分解的方法冶炼 | |
| D. | 若W与Y的原子序数相差5,则二者形成的化合物的化学式一定为Y2W3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com