
【题目】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3 , 不考虑其他杂质) 制取七水合硫酸亚铁(FeSO47H2O),流程如图: 
(1)滤渣Ⅰ的主要成分是(填化学式).
(2)还原时,试剂X若选用SO2 , 则反应后的阴离子是(填化学式).
(3)从分离出滤渣II后的滤液中得到产品,应进行的操作是、、过滤、洗涤、干燥.
(4)七水合硫酸亚铁(FeSO47H2O) 在医学上常用作补血剂.某课外小组通过以下实验方法测定某补血剂中亚铁离子的含量. 步骤a:取10片补血剂样品除去糖衣、研磨、溶解、过滤,将滤液配成250mL溶液;
步骤b:取上述溶液25mL于锥形瓶中,加入少量稀硫酸酸化后,逐渐滴加0.0100mol/L的KMnO4溶液,至恰好完全反应,记录消耗的KMnO4溶液的体积(假定药品中其他成分不与KMnO4反应),发生的反应为:MnO4﹣+5Fe2++8H+=5Fe3++Mn2++4H2O;
步骤c:重复“步骤b”2~3次,平均消耗KMnO4溶液20.00mL.
①步骤a中配制溶液时需要的玻璃仪器除烧杯、胶头滴管外,还需要、 .
②该补血剂中亚铁离子的含量为mg/片 (请写出计算过程).
【答案】
(1)SiO2
(2)SO42﹣
(3)蒸发浓缩;冷却结晶
(4)玻璃棒;250mL容量瓶;56
【解析】解:烧渣中加入稀硫酸,得到硫酸铁、硫酸亚铁和硫酸铝,二氧化硅不反应,过滤,滤渣Ⅰ为二氧化硅,在滤液中加入试剂X,还原硫酸铁得到硫酸铝和硫酸亚铁溶液,调节溶液pH,生成氢氧化铝沉淀,滤渣Ⅱ为氢氧化铝,溶液经蒸发结晶、过滤、洗涤、干燥,可得到FeSO47H2O,(1)二氧化硅不与稀硫酸反应,滤渣1为二氧化硅;
所以答案是:SiO2; (2)试剂X若选用SO2,发生反应:SO2+2Fe3++2H2O=SO42﹣+2Fe2++4H+,则阴离子为SO42﹣;
所以答案是:SO42﹣;(3)滤渣Ⅱ为氢氧化铝,即Al(OH)3,溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可得到FeSO47H2O;
所以答案是:蒸发浓缩;冷却结晶;(4)①配制250mL溶液需要的玻璃仪器除有烧杯、胶头滴管、玻璃棒、250 mL容量瓶;
所以答案是:玻璃棒;250 mL容量瓶;
②MnO4﹣~5Fe2+
25mL溶液中:n(Fe2+)=5 n(MnO4﹣)=5×0.0100mol/L×20.00×10﹣3L=10﹣3 mol,
250 mL溶液中:n(Fe2+)=10﹣3 mol×10=10﹣2mol,
1片补血剂样品中:n(Fe2+)=10﹣3mol,
m(Fe2+)=10﹣3mol×56g/mol=0.056g=56mg;
所以答案是:56.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】根据题意进行计算:
(1)向200mL0.5mol/LAl2(SO4)3溶液中,加入350mL2mol/L NaOH溶液,充分反应后可以得到Al(OH)3沉淀多少g?
(2)若想得到3.9g Al(OH)3沉淀,应向200mL0.5mol/LAl2(SO4)3溶液中加入2mol/L NaOH溶液多少mL?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应P+Q=M+N是放热反应,下列关于反应能量的变化的说法中不正确的是( )
A. 断裂P和Q中化学键吸收的总能量小于形成M和N中化学键释放的总能量
B. P和Q的总能量大于M和N的总能量
C. P和Q的总能量小于M和N的总能量
D. 任何化学反应都伴随着能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质中是同系物的有________;互为同分异构体的有________;互为同素异形体的有________;互为同位素的有________;互为同一物质的有________; (1)液氯 (2)氯气 (3)白磷 (4)红磷 (5)氕 (6)氚 (7) ![]() (8)
(8) ![]() (9)CH2=CH﹣CH3 (10)
(9)CH2=CH﹣CH3 (10) ![]() (11)2,2﹣二甲基丁烷.
(11)2,2﹣二甲基丁烷.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空
(1)有机物 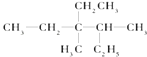 用系统命名法命名:
用系统命名法命名:
(2)写出4甲基2乙基1戊烯的结构简式:
(3)某烃的结构简式是 ![]() ,分子中饱和碳原子数为 , 可能在同一平面上的碳原子数最多为
,分子中饱和碳原子数为 , 可能在同一平面上的碳原子数最多为
(4)下列物质中属于同系物的是
①CH3CH2Cl②CH2═CHCl ③CH3CH2CH2Cl④CH2ClCH2Cl⑤CH3CH2CH2CH3 ⑥CH3CH(CH3)2
A.①②
B.①④
C.①③
D.⑤⑥
(5)0.1mol某烷烃燃烧,其燃烧产物全部被碱石灰吸收,碱石灰增39g.该烃的分子式为;若它的核磁共振氢谱共有3个峰,则该烃可能的结构简式为 . (写出其中一种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质的转化关系如下图所示.B、D是气体,其中B是空气的主要成分之一;C是淡黄色固体,常用于供氧剂;E是红棕色固体;F是最常见的无色液体. 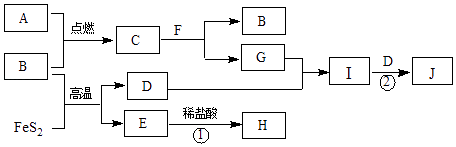
回答下列问题:
(1)C的化学式是 .
(2)气体D通入紫色石蕊溶液的现象是 .
(3)写出反应①的离子方程式 .
(4)写出反应②的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值. 已知:①CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206.2kJmol﹣1
②CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣42.3kJmol﹣1
(1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式为 .
(2)为了探究反应条件对反应CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣42.3kJmol﹣1的影响,某活动小组设计了三个实验,实验曲线如图所示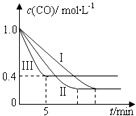
编号 | 温度 | 压强 | c始(CO) | c始(H2O) |
Ⅰ | 530℃ | 3MPa | 1.0molL﹣1 | 3.0molL﹣1 |
Ⅱ | X | Y | 1.0molL﹣1 | 3.0molL﹣1 |
Ⅲ | 630℃ | 5MPa | 1.0molL﹣1 | 3.0molL﹣1 |
①请依据实验曲线图补充完整表格中的实验条件:X=℃,Y=MPa.
②实验Ⅲ从开始至平衡,其平均反应速度率v (CO)=molL﹣1min﹣1 .
③实验Ⅱ达平衡时CO的转化率实验Ⅲ达平衡时CO的转化率(填“大于”、“小于”或“等于”).
④在530℃时,平衡常数K=1,若往10L容器中投入2.0mol CO(g)、2.0mol H2O(g)、1.0mol CO2(g)、1.0mol H2(g),此时化学反应将(填“正向”、“逆向”或“不”) 移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2 , 也可被还原为氢气.为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为101 kPa,温度为0℃).
(1)若在烧瓶中放入1.30g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,量气管的适宜规格是 .
A.200mL
B.400mL
C.500mL
(2)若1.30g锌粒完全溶解,测得盛氢氧化钠溶液的洗气瓶增重1.28g,则圆底烧瓶中发生反应的化学方程式为: .
(3)若烧瓶中投入a g锌且完全反应,氢氧化钠洗气瓶增重b g量气管中收集到VmL气体,其依据得失电子守恒的原理,可得出a、b、V之间的关系为:是 .
(4)若在烧瓶中投入d g锌,再加入VL c mol/L 浓硫酸,充分反应后锌有剩余,测得盛氢氧化钠溶液的洗气瓶增重m g,则整个实验过程产生的混和气体中H2和SO2物质的量之比 ![]() =(用含字母的代数式表示).若撤走盛有无水氯化钙的U型管,
=(用含字母的代数式表示).若撤走盛有无水氯化钙的U型管, ![]() 的比值将(填偏大、偏小或无影响)
的比值将(填偏大、偏小或无影响)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com