
【题目】用下列实验装置进行相应实验,能达到实验目的的是:

A. 用图(a)所示装置除去氯气中含有的少量氯化氢
B. 用图(d)所示装置分离苯萃取碘水后已分层的有机层和水层
C. 用图(c)所示装置制取少量纯净的二氧化碳气体
D. 用图(b)所示装置蒸发氯化钠溶液制备氯化钠晶体
科目:高中化学 来源: 题型:
【题目】按要求填空:有下列物质:①O2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩N2,回答下列问题:
(1)只含有极性键的是________;只含有非极性键的是________;含有极性键和非极性键的是________;只含有离子键的离子化合物是________;含有非极性键的离子化合物是________;
(2)写出⑤、⑧、⑨的电子式_____________、______________、________________;
(3)溶于水只破坏离子键的是__________;溶于水既破坏离子键又破坏共价键的是________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】隔绝空气加热至500℃时硫酸亚铁铵[(NH4)2Fe(SO4)2]能完全分解,分解产物中含有铁 氧化物、硫氧化物、氨气和水蒸气等。
[实验探究]某化学小组选用下图所示部分装置进行分步实验(夹持装置略)。
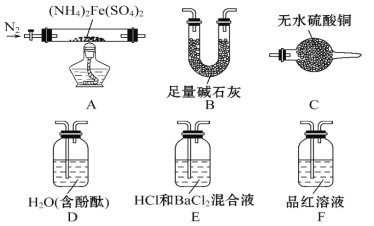
实验Ⅰ 甲同学为探究分解产物中的硫氧化物是 SO2 还是 SO3,连接装置A-E-F-B 进行实验。
(1)实验过程中观察到:E 中没有明显现象,F 中溶液褪色,据此得出的结论是 。
(2)B 的作用是_____。
实验Ⅱ 验证分解产物中含有水蒸气和氨气,并探究残留固体成分。
(3)所选用装置的正确连接顺序为_____(填装置的字母序号)。
(4)证明有水蒸气生成的实验现象为_____。
(5)证明有氨气生成的实验现象为_____。
(6)A 中固体完全分解后变为红棕色粉末,设计实验证明A 中残留固体中含有三价铁_______________。
(7)实验证明(NH4)2Fe(SO4)2 受热分解除上述产物外,还有N2 生成,写出A 中反应的化学方程式__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是一种用途广泛的精细化工产品。某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:
已知:①氯化钙可与乙醇形成CaCl2·6C2H5OH
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
③2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
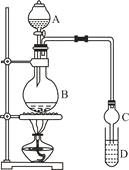
I.制备过程
装置如图所示,A中放有浓硫酸,B中放有9.5mL无水乙醇和6mL冰醋酸,D中放有饱和碳酸钠溶液。
(1)写出乙酸与乙醇发生酯化反应的化学方程式 。
(2)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是 (填入正确选项前的字母)
A.25mL B.50mL C.250mL D.500mL
(3)球形干燥管的主要作用是 。
(4)预先向饱和Na2CO3溶液中滴加几滴酚酞试液,目的是
。
Ⅱ.提纯方法:①将D中混合液转入分液漏斗进行分液。
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤。有机层倒入一干燥的烧瓶中,用无水硫酸镁干燥,得粗产物。
③将粗产物蒸馏,收集77.1℃的馏分,得到纯净干燥的乙酸乙酯。
(5)第①步分液时,选用的两种玻璃仪器的名称分别是 、 。
(6)第②步中用饱和食盐水、饱和氯化钙溶液、最后用水洗涤,分别主要洗去粗产品中的 , , 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,配制一组c(Na2CO3)+c(NaHCO3)=0.100 mol·L-1的混合溶液,溶液中c(HCO3-)、c(CO32-)与pH的关系如右图所示。下列指定溶液中微粒的物质的量浓度关系正确的是

A. pH=9的溶液中:c(HCO3-)>c(H2CO3)+c(CO32-)
B. c(HCO3-)= c(CO32-)的E点溶液中:c(OH-)+c(CO32-)>c(H+)+ c(H2CO3) +0.050 mol·L-1
C. pH=11的溶液中:c(Na+)<2c(CO32-)+c(HCO3-)
D. 0.100 mol·L-1的Na2CO3溶液中:c(H+)+c(H2CO3) + c(HCO3-)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯乙烯(b)、立方烷(d)、环辛四烯(p)的分子式均为C8H8。下列说法正确的是

A. b、d的二氯代物均只有三种 B. b、p均能与酸性高锰酸钾溶液反应
C. d是烷烃,只能取代,不能加成 D. b和苯乙炔一样,所有原子一定处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在新制氯水中滴加NaOH 溶液,溶液中水电离出来的c水(H+)的对数与NaOH 溶液体积之间的关系如图所示。下列推断正确的是

A. 用pH试纸测定E点对应的溶液,其pH=3
B. F、H点对应的溶液中都存在c(Na+)=c(Cl-)+c(ClO-)
C. G点对应的溶液中c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+)
D. 加水稀释H点对应的溶液,溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:

(1)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式是:______________ 、________________;
(2)第③步中,生成氢氧化铝的离子方程式是_____________。若往A溶液中通入足量CO2,产生的沉淀为____________________(填化学式);
(3)工业上制取AlCl3常用Al2O3与C、Cl2在高温条件下反应,已知每消耗0.5mol碳单质,转移1mol电子,则该反应的氧化产物为_____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物和硫的氧化物是导致酸雨的物质。
(1)SO2有毒,且能形成酸雨,是大气主要污染物之一。石灰-石膏法和碱法是常用的烟气脱硫法。石灰-石膏法的吸收原理:
①SO2+Ca(OH)2=CaSO3↓+H2O②2CaSO3+O2+4H2O=2(CaSO4·2H2O)碱法的吸收原理:将含SO2的尾气通入足量的烧碱溶液中,请写出对应的化学反应方程式__________;
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
和石灰-石膏法相比,碱法的优点是吸收快、效率高,缺点是__________;
(2)石灰-石膏法和碱法的基础上,设计了双碱法,能实现物料循环利用。

上述方法中,实现循环利用的物质是__________,请用化学方程式表示在Na2SO3溶液中加入CaO后的反应原理__________。
(3)一定条件下氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:____________
(4)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O
2NO2+2NaOH=NaNO2+NaNO3+H2O
现有VL某NaOH溶液能完全吸收n mol NO2和m mol NO组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为________mol·L-1。
②若所得溶液中c(NO3-)∶c(NO2-)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com