
| A.随着电解的进行,c(NaCl)降低,需不断补充饱和食盐水 |
| B.电解过程中采用增大阳极区溶液pH的方法,可以减少Cl2在水中的溶解量 |
| C.阳离子交换膜的作用是阻止OH-移向阳极,以使氢氧化钠在阴极区富集 |
| D.阳极表面用钛氧化物涂层处理,目的是降低电解产物Cl2对电极的腐蚀 |
科目:高中化学 来源:不详 题型:单选题
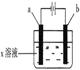
| | a电极 | b电极 | x溶液 | 实 验 现 象 |
| A | 石墨 | 石墨 | CuCl2 | a极质量增加,b极放出无色气体 |
| B | Fe | 石墨 | KNO3 | a极质量增加,b极放出无色气体 |
| C | Fe | Cu | CuSO4 | a极质量增加,b极质量减少 |
| D | 石墨 | 石墨 | HCl | a极放出无色气体,b极放出无色气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
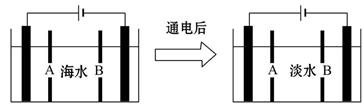
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
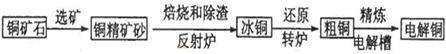
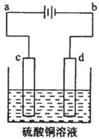
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 2HX(g) (X2表示Cl2、Br2和I2)。
2HX(g) (X2表示Cl2、Br2和I2)。 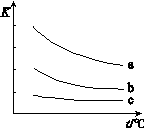

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
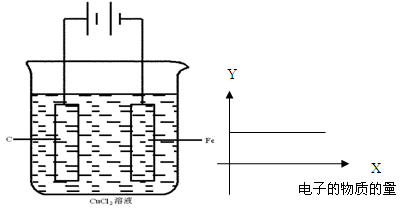
| A.Cu2+物质的量浓度 | B.C棒的质量 |
| C.Fe棒的质量 | D.Cl-物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.12LH2 | B.1.12LO2 | C.2.24LH2 | D.2.24LO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
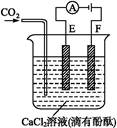
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com