
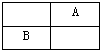
| A、A一定是第2周期元素 |
| B、B的原子半径一定比A大 |
| C、B的金属性一定比A强 |
| D、A的熔沸点一定比B高 |


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
| A、生成盐和水的反应一定是中和反应 |
| B、复分解反应一定没有单质参加 |
| C、生成一种单质和一种化合物的反应一定是置换反应 |
| D、两种酸之间一定不能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
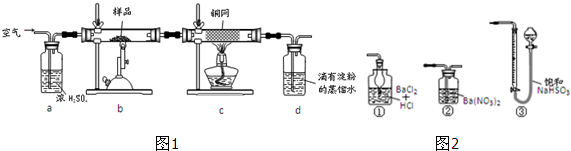
| 1 |
| 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol任何纯净物都含有相同的分子数 |
| B、1 mol氦气中约含有6.02×1023个氦原子 |
| C、1 mol水中含有8mol电子 |
| D、1 molNa的质量为23 g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 铜 |
| B | 胆矾 | 石灰水 | 硫酸钡 | NH3 |
| C | 火碱 | 蔗糖溶液 | 氯化钠溶液 | 三氧化硫 |
| D | 纯醋酸 | 氢氧化铁胶体 | 苛性钾溶液 | 乙醇 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com