
【题目】下列变化中,必须加入氧化剂才能发生的是( )
A.SO2→SB.SO32-→SO2C.I-→I2D.KClO3 →O2
科目:高中化学 来源: 题型:
【题目】下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。请回答下列问题:
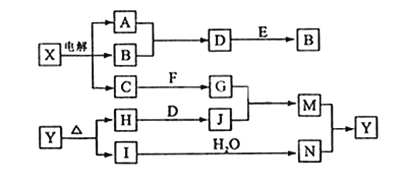
(1)B中所含元素位于周期表中第____周期____族。
(2)A在B中燃烧的现象是_______________。
(3)D+E→B的反应中,被氧化与被还原的物质的物质的量比是________。
(4)G+J→M的离子方程式是 _________________。
(5)Y受热分解的化学方程式是 ___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到目的的是

A. 装置①依据褪色快慢探究浓度对反应速率的影响 B. 装置②可用于测定中和热
C. 装置③探究Mg(OH)2能否转化成Fe(OH)3 D. 装置④构成锌—铜原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠离子电池正成为化学电源的新宠。
(1)有一种新型的高能电池—钠硫电池(熔融的钠、硫为两极,以Na+导电的βAl2O3陶瓷作固体电解质),反应式为2Na+xS ![]() Na2Sx。
Na2Sx。
①充电时,钠极与外电源________(填“正”或“负”)极相连。其阳极反应式:_____________。
②用该电池作电源电解(如图)NaCl溶液(足量),写出电解NaCl溶液的离子方程式:________________________________。

③若用该钠硫电池作电源在一铁片上镀铜,此铁片与__________(填“钠”或“硫”)极相连。
(2)“Na-CO2”电池可将CO2变废为宝。我国科研人员研制出的可充电“ Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2 ![]() 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:

①放电时,正极的电极反应式为_____________________________。
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2 mol e-时,两极的质量差为________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用热的氢氧化钠溶液洗去试管内壁沾有的硫单质,发生反应6NaOH+3S![]() 2Na2S+Na2SO3+3H2O。关于该反应的说法不正确的是( )
2Na2S+Na2SO3+3H2O。关于该反应的说法不正确的是( )
A. 硫既是氧化剂又是还原剂 B. 硫化钠是还原产物
C. 硫既表现氧化性又表现还原性 D. 消耗3 mol 硫,转移电子6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量的铁粉加入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+的物质的量浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比( )
A.3︰2B.1︰2C.2︰1D.2︰3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用下列化学反应在实验室中制备氯气,并进行有关氯气性质的研究。MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)该小组同学欲用下图所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。


①应该选择的仪器是________(填字母)。
②浓盐酸与二氧化锰反应的离子方程式为____________________________
(2)该小组同学设计并分别利用下图所示装置探究氯气的氧化性。

①G中的现象是________,原因是__________________(用化学方程式表示)。
②H中的现象是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7∶17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是( )
A. 氢化物的稳定性:X>WB. 金属性:Y>Z
C. 非金属性:W>XD. 原子半径:Y>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是

A. 正极反应为AgCl +e-=Ag +Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com