
【题目】A、F、B、C、D、E、W为六种前四周期元素,它们的原子序数依次增大。A与D同主族,可形成DA型离子化合物,F、B与C同周期且相邻,C与E同主族,E2-与Ar原子具有相同的电子层结构,W的合金用量最大、用途最广。请回答下列问题:
(1)W在元素周期表中的位置______________________;DA的电子式_______________
(2)A分别与C、E形成最简单化合物中沸点较高的是______________(填化学式),原因是_____________。
(3)A、C、D三种元素形成的物质中含有的化学键类型___________________,
(4)A、F、B、C四种元素形成化合物A8F2B2C4,其化学式为______________。
(5)向盛有A2C2溶液的试管中加入几滴酸化的WEC4溶液,溶液变成棕黄色,发生反应的离子方程式为___________________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成,产生气泡的原因是_____________;生成沉淀的原因是_______________________________(用平衡移动原理解释)。
【答案】 第四周期 VIII族 ![]() H2O 水分子间存在氢键 离子键、共价键(或极性共价键) (NH4)2 C2O4 H2O2+2H++2Fe2+=2Fe3++2H2O Fe3+催化H2O2分解产生O2 H2O2分解反应放热,促进Fe3+水解平衡向正向移动
H2O 水分子间存在氢键 离子键、共价键(或极性共价键) (NH4)2 C2O4 H2O2+2H++2Fe2+=2Fe3++2H2O Fe3+催化H2O2分解产生O2 H2O2分解反应放热,促进Fe3+水解平衡向正向移动
【解析】A、F、B、C、D、E、W为六种前四周期元素,它们的原子序数依次增大。E2-与Ar原子具有相同的电子层结构,则E为S元素;C与E同主族,则C为O元素;F、B与C同周期且相邻,则B为N元素,F为C元素;A与D同主族,可形成DA型离子化合物,二者只能处于IA族,结合原子序数可知A为H元素,D为Na;W的合金用量最大、用途最广,则W为Fe。
(1)W为Fe元素,在元素周期表中的位置为:第四周期第Ⅷ族,氢化钠的电子式为![]() ,故答案为:第四周期第Ⅷ族;
,故答案为:第四周期第Ⅷ族;![]() ;
;
(2)A分别与C、E形成最简单化合物分别为H2O、H2S,由于水分子间存在氢键,H2O的沸点较高,故答案为:H2O;水分子间存在氢键;
(3)A、C、D三种元素形成的物质为NaOH,含有的化学键有离子键、共价键,故答案为:离子键、共价键;
(4)A、F、B、C四种元素形成化合物A8F2B2C4的化学式为(NH4)2 C2O4,故答案为:(NH4)2 C2O4;(5)向盛有H2O2溶液的试管中加入几滴酸化的FeSO4溶液,溶液变成棕黄色,发生反应的离子方程式为:H2O2+2H++2Fe2+=2Fe3++2H2O;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成,产生气泡的原因是:Fe3+催化H2O2分解产生O2 ;生成沉淀的原因是:H2O2分解反应放热,促进Fe3+水解平衡向正向移动,故答案为:H2O2+2H++2Fe2+=2Fe3++2H2O;Fe3+催化H2O2分解产生O2 ;H2O2分解反应放热,促进Fe3+水解平衡向正向移动。


科目:高中化学 来源: 题型:
【题目】金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3 (s) + 3H2 (g) ![]() W (s) + 3H2O (g)
W (s) + 3H2O (g)
请回答下列问题:
(1)上述反应的化学平衡常数表达式为___________________________。
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为_____;随温度的升高,H2与水蒸气的体积比减小,则该反应为反应_______(填“吸热”或“放热”)。
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
温度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
主要成份 | WO3 W2O5 WO2 W |
第一阶段反应的化学方程式为_____________;
580℃时,固体物质的主要成分为________;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为____________。
(4)已知:温度过高时,WO2 (s)转变为WO2 (g);
WO2 (s) + 2H2 (g) ![]() W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
WO2 (g) + 2H2(g) ![]() W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
则WO2 (s) ![]() WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某2 L恒容密闭容器中充入2 mol X(g)和1 mol Y(g)发生反应:2X(g)+Y(g)![]() 3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
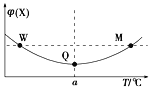
A. M点时,Y的转化率最大
B. W、M两点Y的正反应速率相等
C. 升高温度,平衡常数减小
D. 平衡后充入Z达到新平衡时Z的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是
A. 实验室制备氢气 B. 灼热的碳与水的反应
C. Ba(OH)2·8H2O与NH4Cl的反应 D. 铝粉与氧化铁粉末反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解足量的NaCl溶液一段时间后,欲使溶液恰好恢复至电解前情况,可加入的物质是
A. NaCl B. H2O C. 盐酸 D. HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能说明NH3·H2O一定是弱电解质的是
①常温下,NH3·H2O溶液能使酚酞变红; ②用NH3·H2O溶液做导电性实验,灯泡很暗;
③常温下,0.1mol / L氯化铵溶液的pH约为5
④常温下,体积相同且pH相同的NH3·H2O溶液和NaOH溶液,与相同浓度的HCl溶液中和时,消耗HCl溶液的体积:前者>后者
A.①②③④ B.②③④ C.③④ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%浓硫酸配制2mol/L的稀硫酸,下列情况会使所配溶液浓度偏低的是( )
A.未冷却就转移、定容
B.容量瓶原有少量蒸馏水
C.定容时俯视刻度线观察液面
D.量筒取浓盐酸时,俯视读数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com